题目内容
下列各组物质,按单质、化合物、混合物顺序排列的是( )
| A、生石灰、白磷、熟石灰 |
| B、液态氧、碘酒、烧碱 |
| C、铁、氯化氢、干冰 |
| D、氮气、胆矾、空气 |
考点:单质和化合物,混合物和纯净物
专题:
分析:只有一种元素组成的纯净物是单质,由两种元素组成的纯净物属于化合物,由多种元素组成的物质属于混合物.
解答:
解:A、生石灰是氧化钙,属于化合物,故A错误;
B、碘酒属于混合物,故B错误;
C、干冰属于化合物,故C错误;
D、氮气、胆矾、空气分别属于单质,氧化物和混合物,故D正确,
故选D.
B、碘酒属于混合物,故B错误;
C、干冰属于化合物,故C错误;
D、氮气、胆矾、空气分别属于单质,氧化物和混合物,故D正确,
故选D.
点评:本题主要考查的是物质的分类,了解单质与化合物的元素组成以及混合物的物质组成是解决本题的关键,难度不大.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
下列反应中,生成物的总能量大于反应物的总能量的是( )
| A、铝与稀盐酸的反应 |
| B、焦炭在高温下与水蒸气反应 |
| C、硫在氧气中燃烧 |
| D、氢氧化钠与盐酸的反应 |
下列表达方式错误的是 ( )
A、O-18原子的符号:
| ||
B、S2-的结构示意图: | ||
C、氯化氢分子的电子式:H+[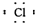 ]- ]- | ||
| D、CO2分子的结构式:O=C=O |
下列热化学方程式或离子方程式中,正确的是( )
| A、甲烷的标准燃烧热为-890.3kJ?mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ?mol-1 | ||||
B、500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)
| ||||
| C、氯化镁溶液与氨水反应:Mg2++2OH-═Mg(OH)2↓ | ||||
| D、氧化铝溶于NaOH溶液:Al2O3+2OH-+3H2O═2Al(OH)4- |
下列物质的电子式书写正确的是( )
A、NaCl  |
B、H2S  |
C、NF3 |
D、NH4I  |
工业上消除氮氧化物的污染,可用如下反应:CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)△H=a kJ/mol 在温度T1和T2时,分别将0.50mol CH4和1.2mol NO2充入体积为1L的密闭容器中,测得n(CH4)随时间变化数据如下表:下列说法不正确的是( )
| 温度 | 时间/min n/mol | 0 | 10 | 20 | 40 | 50 |
| T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| T2 | n(CH4) | 0.50 | 0.30 | 0.18 | … | 0.15 |
| A、10 min内,T1时CH4的化学反应速率比T2时小 |
| B、温度:T1<T2 |
| C、a<0 |
| D、平衡常数:K(T1)<K(T2) |
恒温下,容积均为2L的密闭容器M、N中,分别有以下列两种起始投料建立的可逆反应3A(g)+2B(g)?2C(g)+xD(s)的化学平衡状态,相关数据如下:M:3molA、2molB;2min;达到平衡,生成D1.2mol,测得从反应开始到平衡C的速率为0.3mol/Lmin.N:2molC、ymolD;达到平衡时c(A)=0.6mol/L.下列推断的结论中不正确的是( )
| A、x=2 |
| B、平衡时M中c(A)=0.6mol/L |
| C、y<0.8 |
| D、M中B的转化率与N中C的转化率之和为1 |

