题目内容
下列有关实验操作、发生的现象、解释或结论都正确的是( )
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | 向AgCl沉淀中滴加KI溶液 | 沉淀变为黄色 | Ksp(AgCl)>Ksp(AgI) |
| B | 将SO2通入滴有酚酞的 NaOH溶液中 | 溶液红色褪去 | SO2具有漂白性 |
| C | 常温下铜片插入浓硫酸中 | 无明显现象 | 常温下铜遇浓硫酸钝化 |
| D | 向某溶液中加入过量盐酸 | 产生能使澄清石灰水变浑浊的无色气体 | 该溶液中一定含有CO32- |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:
分析:A.发生沉淀的转化;
B.二氧化硫是酸性氧化物;
C.铜的活泼性比氢弱;
D.能够使澄清石灰水变浑浊的气体有二氧化硫和二氧化碳,所以溶液中可能含有亚硫酸根离子、碳酸氢根离子等.
B.二氧化硫是酸性氧化物;
C.铜的活泼性比氢弱;
D.能够使澄清石灰水变浑浊的气体有二氧化硫和二氧化碳,所以溶液中可能含有亚硫酸根离子、碳酸氢根离子等.
解答:
解:A.向AgCl沉淀中滴加KI溶液,白色沉淀转化为黄色沉淀,发生沉淀的转化,说明溶度积为AgI比AgCl更小,故A正确;
B.二氧化硫是酸性氧化物,能与氢氧化钠反应生成亚硫酸钠或亚硫酸氢钠,与漂白性无关,故B错误;
C.铜的活泼性比氢弱,与硫酸不反应,未发生钝化,故C错误;
D.某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,该气体可能为二氧化碳、二氧化硫,溶液中可能存在亚硫酸根离子、亚硫酸氢根离子、碳酸氢根离子,所以该溶液中不一定存在大量CO32-,故D错误.
故选A.
B.二氧化硫是酸性氧化物,能与氢氧化钠反应生成亚硫酸钠或亚硫酸氢钠,与漂白性无关,故B错误;
C.铜的活泼性比氢弱,与硫酸不反应,未发生钝化,故C错误;
D.某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,该气体可能为二氧化碳、二氧化硫,溶液中可能存在亚硫酸根离子、亚硫酸氢根离子、碳酸氢根离子,所以该溶液中不一定存在大量CO32-,故D错误.
故选A.
点评:本题考查化学实验方案的评价,涉及沉淀转化、物质的性质、离子的检验,侧重物质性质的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
Al2O3MgO混合物溶于250mL盐酸得到无色溶液,逐滴加入0.5moL/LNaoH溶液,如图下列说法错误的是( )


| A、盐酸的物质的量浓度为0.22mol/L |
| B、混合物中Al2O3的物质的量为0.01mol |
| C、混合物中MgO的物质的量为0.01mol |
| D、P点加入NaOH溶液的体积是110mL |
下列说法不正确的是( )
A、 的分子式为C17H24O3 的分子式为C17H24O3 |
| B、水溶液中氨基酸在等电点时的溶解度最小.不同的氨基酸达到等电点的pH不同,故可以通过调节溶液pH分离某些氨基酸 |
C、有机硅聚醚( )可由单体 )可由单体  和 和 缩聚而成 缩聚而成 |
| D、等质量的甲醇、甲醛、甲醚完全燃烧时的耗氧量依次递增 |
下列各组离子在溶液中不能大量共存的是( )
| A、H2PO4-、NH4+、K+、Mg2+ |
| B、Mg2+、Na+、Cl-、F- |
| C、H+、Cl-、SO42-、K+ |
| D、K+、Zn2+、Br-、NO3- |
某无色溶液中,常温下由水电离出的c(H+)=1×10-14 mol/L,则该溶液中一定能大量共存的离子是( )
| A、Al3+、Na+、MnO4-、SO42- |
| B、Na+、Ag+、Cl-、NO3-、 |
| C、Na+、K+、Cl-、NO3- |
| D、K+、Ba2+、Cl-、HCO3- |
化学与生产、生活密切相关.下列叙述正确的是( )
| A、明矾净水和家用消毒剂的消毒原理相同 |
| B、使用含有氯化钠的融雪剂会加快桥梁的腐蚀 |
| C、铝合金的广泛使用是因为人们能用焦炭等还原剂从氧化铝中获取铝 |
| D、钒氮合金钢是“鸟巢”的主要材料之一,其熔点、硬度和强度均高于纯铁 |
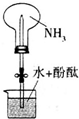 化学是一门以实验为基础的科学.
化学是一门以实验为基础的科学.