题目内容
X、Y和Z三种短周期元素,原子序数之和为32,X和Y为相邻周期的元素,Y和Z为相同周期的元素.Y的质子数比X多5个,X的最外层电子数为Y的最外层电子数的2倍,X的最外层电子数和Z的最外层电子数之和为7,下列叙述中不正确的是( )
| A、X和Y两种元素构成一种阴离子,该阴离子与强酸反应时,可能变成Y的阳离子 |
| B、元素Y的最高价氧化物能溶于Z的最高价氧化物的水化物中 |
| C、X、Y和Z三元素组成的化合物为碱 |
| D、X与Z的单质在不同条件下能生成不同的化合物 |
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:X、Y、Z为三种短周期元素,即在前三周期,X和Y为相邻周期的元素,Y的质子数比X多5个,则X、Y在第一周期和第二周期或在第二周期和第三周期,如果X、Y在第一周期和第二周期,由于X的最外层电子数为Y最外层电子数的2倍,则X最外层只能是2,即为氦元素,Y的质子数比X多5个,即Y为7号氮元素,而此时最外层不能满足2倍的关系,故X在第二周期、Y在第三周期,设Y元素的最外层电子数为a,则X元素的最外层电子数为2a,根据Y的质子数比X多5个,有2+8+a-(2+2a)=5,得a=3,可知X元素为8号元素氧元素、Y为13号元素铝元素,由X、Y、Z原子序数之和为32,所以Z为11号元素,即钠元素,据此答题即可.
解答:
解:依据分析可知X为氧,Y为铝,Z为钠,
A、O和Al两种元素构成一种阴离子:AlO2-,AlO2-与强酸反应时,可能变成Al3+,故A正确;
B、元素Al的最高价氧化物:氢氧化铝,氢氧化铝能溶于NaOH,故B正确;
C、O、Al和Na三元素组成的化合物:偏铝酸钠,偏铝酸钠为盐,故C错误;
D、O与Na的单质常温下生成氧化钠,加热生成过氧化钠,故D正确,故选C.
A、O和Al两种元素构成一种阴离子:AlO2-,AlO2-与强酸反应时,可能变成Al3+,故A正确;
B、元素Al的最高价氧化物:氢氧化铝,氢氧化铝能溶于NaOH,故B正确;
C、O、Al和Na三元素组成的化合物:偏铝酸钠,偏铝酸钠为盐,故C错误;
D、O与Na的单质常温下生成氧化钠,加热生成过氧化钠,故D正确,故选C.
点评:本题主要考查了根据元素在周期表中的位置及原子结构特点推断元素种类,中等难度,解题的难点在X、Y元素的确定.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法错误的是( )
| A、在溶液中,导电能力弱的电解质不一定是弱电解质 |
| B、强电解质都是离子化合物,弱电解质都是共价化合物 |
| C、纯净的强电解质在液态时,有的导电,有的不导电 |
| D、虽然SO2的水溶液能导电,但是SO2是非电解质 |
下列反应中,观察不到颜色变化的是( )
| A、往氨水中滴加酚酞 |
| B、往稀硫酸中通入氨气 |
| C、往品红溶液中通人足量二氧化硫气体 |
| D、氯气通入淀粉碘化钾溶液中 |
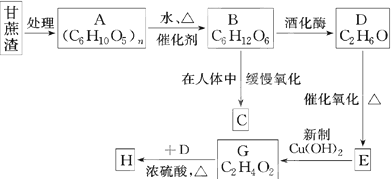
高氯酸铵(NH4ClO4)是复合火箭推进剂的重要成分,实验室可通过下列途径制取:

已知NaClO4与NH4Cl投入的物质的量之比为1:1,相关物质的溶解度随温度变化如图所示,下列说法不正确的是( )
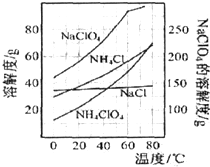

已知NaClO4与NH4Cl投入的物质的量之比为1:1,相关物质的溶解度随温度变化如图所示,下列说法不正确的是( )

| A、制得粗产品的反应原理为:NH4Cl+NaClO4=NaCl+NH4ClO4↓ |
| B、上述流程中操作Ⅰ为冷却结晶,操作Ⅱ为重结晶 |
| C、洗涤粗产品时,宜用冷水洗涤 |
| D、上述流程中蒸发浓缩时,蒸发至剩余少量溶液时,应停止加热,利用余热将其蒸干,防止晶体飞溅 |

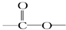 链状结构的同分异构体最多有
链状结构的同分异构体最多有