题目内容
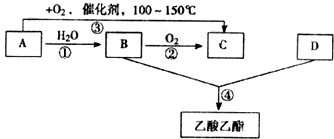 已知:A是石油裂解气的主要成份.A的产量通常用来衡量一个国家的石油化工水平,现以A为主要原料合成乙酸乙酯,其合成路线如图所示.
已知:A是石油裂解气的主要成份.A的产量通常用来衡量一个国家的石油化工水平,现以A为主要原料合成乙酸乙酯,其合成路线如图所示.(1)写出A的电子式
(2)B和D分子中的官能团名称分别是
(3)写出下列反应的反应类型:
①
②
④
(4)写出下列反应的化学方程式
①
②
④
考点:有机物的推断
专题:有机物的化学性质及推断
分析:A是石油裂解气的主要成份,其产量通常用来衡量一个国家的石油化工水平,则A是乙烯,乙烯和水发生加成反应生成B为乙醇,乙醇和氧气反应生成C,乙烯在催化剂、加热条件下也可以氧化得到C,则C是乙醛,乙醇与D反应生成乙酸乙酯,则D是乙酸,据此解答.
解答:
解:A是石油裂解气的主要成份,其产量通常用来衡量一个国家的石油化工水平,则A是乙烯,乙烯和水发生加成反应生成B为乙醇,乙醇和氧气反应生成C,乙烯在催化剂、加热条件下也可以氧化得到C,则C是乙醛,乙醇与D反应生成乙酸乙酯,则D是乙酸,
(1)A为乙烯,其电子式为 ,故答案为:
,故答案为: ;
;
(2)B为乙醇,含有官能团为羟基,D为乙酸,含有官能团为羧基,故答案为:羟基;羧基;
(3)反应①是乙烯与水发生加成反应生成乙醇,反应②是乙醇发生氧化反应生成乙醛,反应④是乙醇与乙酸发生酯化反应生成乙酸乙酯,也属于取代反应,
故答案为:加成;氧化;酯化或取代;
(4)反应①的化学反应方程式为:CH2=CH2+H2O
CH3CH2OH,
反应②的化学反应方程式为:2CH3CH2OH+O2
2CH3CHO+2H2O,
反应④的化学反应方程为:CH3CH2OH+CH3COOH
CH3COOCH2CH3+H2O,
故答案为:CH2=CH2+H2O
CH3CH2OH;2CH3CH2OH+O2
2CH3CHO+2H2O;
CH3CH2OH+CH3COOH
CH3COOCH2CH3+H2O.
(1)A为乙烯,其电子式为
 ,故答案为:
,故答案为: ;
;(2)B为乙醇,含有官能团为羟基,D为乙酸,含有官能团为羧基,故答案为:羟基;羧基;
(3)反应①是乙烯与水发生加成反应生成乙醇,反应②是乙醇发生氧化反应生成乙醛,反应④是乙醇与乙酸发生酯化反应生成乙酸乙酯,也属于取代反应,
故答案为:加成;氧化;酯化或取代;
(4)反应①的化学反应方程式为:CH2=CH2+H2O
| 催化剂 |
反应②的化学反应方程式为:2CH3CH2OH+O2
| Cu |
| △ |
反应④的化学反应方程为:CH3CH2OH+CH3COOH
| 浓硫酸 |
| △ |
故答案为:CH2=CH2+H2O
| 催化剂 |
| Cu |
| △ |
CH3CH2OH+CH3COOH
| 浓硫酸 |
| △ |
点评:本题考查有机物的推断,涉及烯、醇、醛、羧酸等的性质与转化等,难度不大,注意对基础知识的理解掌握.

练习册系列答案
相关题目
下列各项操作中,不发生“先产生沉淀,然后沉淀又溶解”现象的是( )
①向饱和碳酸钠溶液中通入过量CO2
②向NaAlO2溶液中逐滴加入过量的稀盐酸
③向AlCl3溶液中逐滴加入过量稀NaOH溶液
④向硅酸钠溶液中逐滴加入过量的盐酸
⑤向AgNO3溶液中逐滴加入稀氨水.
①向饱和碳酸钠溶液中通入过量CO2
②向NaAlO2溶液中逐滴加入过量的稀盐酸
③向AlCl3溶液中逐滴加入过量稀NaOH溶液
④向硅酸钠溶液中逐滴加入过量的盐酸
⑤向AgNO3溶液中逐滴加入稀氨水.
| A、①② | B、②③ | C、①④ | D、④⑤ |
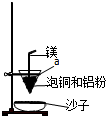
实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是( )、
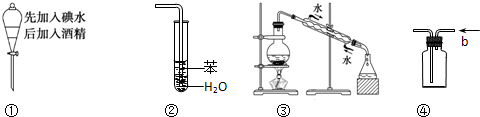

| A、溶液上层无色,下层紫红色 |
| B、装置②可用于吸收HCl气体,并防止倒吸 |
| C、装置③可用于制取蒸馏水 |
| D、装置④b口进气可收集H2、CO2等气体 |
海水是一个巨大的化学资源宝库,下列有关海水综合利用的说法,正确的是( )
| A、海水中含有镁元素,只需经过物理变化就可以得到镁单质 |
| B、海水蒸发制海盐的过程中只发生了化学变化 |
| C、从海水中可以得到NaCl,电解NaCl溶液可得到金属钠 |
| D、从海水中提取Br2、I2的过程中发生了氧化还原反应 |
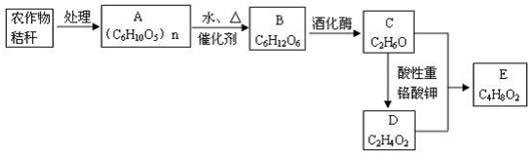
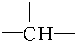 和1个-OH.则B可能结构有4种,已知其中2种结构简式为
和1个-OH.则B可能结构有4种,已知其中2种结构简式为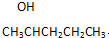 、
、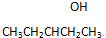 ,请写出另外两种
,请写出另外两种