题目内容
现有一定量含有Na2O杂质的Na2O2试样,用下图所示的实验装置测定Na2O2试样的纯度.(可供选用的试剂只有CaCO3固体、6mol/L盐酸、6mol/L硫酸和蒸馏水)
回答下列问题:
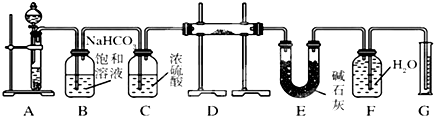
(1)装置A中液体试剂选用 ,理由是 .
(2)装置B的作用是 ,装置E中碱石灰的作用是 .
(3)装置D中发生反应的化学方程式是: 、 .
(4)若开始时测得样品的质量为2.0g,反应结束后测得气体体积为224mL(标准状况),则Na2O2试样的纯度为 .
回答下列问题:

(1)装置A中液体试剂选用
(2)装置B的作用是
(3)装置D中发生反应的化学方程式是:
(4)若开始时测得样品的质量为2.0g,反应结束后测得气体体积为224mL(标准状况),则Na2O2试样的纯度为
考点:实验装置综合
专题:实验设计题
分析:(1)根据实验原理装置A采用的是碳酸钙和盐酸反应生成二氧化碳,根据碳酸钙和硫酸反应的情况来回答;
(2)B中饱和的碳酸氢钠溶液可以吸收HCl,但是不吸收二氧化碳;E中碱石灰可以吸收二氧化碳;
(3)根据氧化钠和过氧化钠的性质来回答;
(4)根据氧气的量和过氧化钠量的关系来获得过氧化钠质量,进而计算过氧化钠的纯度.
(2)B中饱和的碳酸氢钠溶液可以吸收HCl,但是不吸收二氧化碳;E中碱石灰可以吸收二氧化碳;
(3)根据氧化钠和过氧化钠的性质来回答;
(4)根据氧气的量和过氧化钠量的关系来获得过氧化钠质量,进而计算过氧化钠的纯度.
解答:
解:(1)装置A是碳酸钙和盐酸反应生成二氧化碳,碳酸钙和硫酸反应时,生成的硫酸钙是微溶于水的,会覆盖在碳酸钙的表面,使反应不能持续,所以用盐酸而不用硫酸来反应,
故答案为:6mol/L盐酸;A的目的是制取CO2,硫酸与CaCO3固体反应生成CaSO4微溶于水,会覆盖在CaCO3固体表面,使反应不能持续;
(2)B中饱和的碳酸氢钠溶液可以吸收HCl,但是不吸收二氧化碳,碳酸钙和盐酸反应生成的二氧化碳气体中含有氯化氢气体,可以用饱和碳酸氢钠来除去;浓硫酸具有吸水性,可以将二氧化碳干燥,装置E中碱石灰的作用是吸收二氧化碳,防止水蒸气进入D中,防止对氧气的体积测量造成干扰;
故答案为:除去气体中的HCl;吸收装置D中反应剩余的CO2、防止水蒸气进入D中;
(3)装置D中氧化钠和过氧化钠和二氧化碳反应的原理方程式分别为:2Na2O2+2CO2=2Na2CO3+O2,Na2O+CO2=Na2CO3,
故答案为:2Na2O2+2CO2=2Na2CO3+O2、Na2O+CO2=Na2CO3;
(4)根据反应2Na2O2+2CO2=2Na2CO3+O2,反应结束后测得气体体积为224mL(标准状况),即生成的氧气的量为
=0.01mol,过氧化钠的物质的量为0.02mol,过氧化钠的纯度=
×100%=78%,
故答案为:78%.
故答案为:6mol/L盐酸;A的目的是制取CO2,硫酸与CaCO3固体反应生成CaSO4微溶于水,会覆盖在CaCO3固体表面,使反应不能持续;
(2)B中饱和的碳酸氢钠溶液可以吸收HCl,但是不吸收二氧化碳,碳酸钙和盐酸反应生成的二氧化碳气体中含有氯化氢气体,可以用饱和碳酸氢钠来除去;浓硫酸具有吸水性,可以将二氧化碳干燥,装置E中碱石灰的作用是吸收二氧化碳,防止水蒸气进入D中,防止对氧气的体积测量造成干扰;
故答案为:除去气体中的HCl;吸收装置D中反应剩余的CO2、防止水蒸气进入D中;
(3)装置D中氧化钠和过氧化钠和二氧化碳反应的原理方程式分别为:2Na2O2+2CO2=2Na2CO3+O2,Na2O+CO2=Na2CO3,
故答案为:2Na2O2+2CO2=2Na2CO3+O2、Na2O+CO2=Na2CO3;
(4)根据反应2Na2O2+2CO2=2Na2CO3+O2,反应结束后测得气体体积为224mL(标准状况),即生成的氧气的量为
| 0.224L |
| 22.4L/mol |
| 0.02mol×78g/mol |
| 2.0g |
故答案为:78%.
点评:本题考查学生过氧化钠的化学性质知识,通过实验方式考查增加了难度,综合性较强.注意硫酸钙的微溶性,主要从反应原理和装置特点分析,题目难度中等.

练习册系列答案
相关题目
下列装置或操作能达到实验目的是( )
A、 除去CO2中的HCl |
B、 稀释浓硫酸 |
C、 检查装置气密性 |
D、 实验室制备乙烯 实验室制备乙烯 |
下列变化(现象)的原理相同的是( )
| A、浓硫酸和浓盐酸敞口存放浓度均变小 |
| B、将单质铁和铜分别与单质硫加热反应均生成低价硫化物(FeS和Cu2S) |
| C、在过氧化氢水溶液中加入二氧化锰、在盛有锌粒和稀硫酸的溶液中滴加硫酸铜溶液,产生气体的速率均加快 |
| D、将氯化铝溶液和碳酸氢钠溶液分别用酒精灯加热蒸干,然后灼烧,最后均得到白色固体 |
下列各组离子在指定溶液中,能大量共存的是( )
| A、pH=0溶液:Fe3+、Mg2+、SO42-、NO3- |
B、滴加甲基橙显红色的溶液:Ca2+、K+、MnO4-、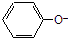 |
| C、1mol?L-1KI溶液中:Cu2+、Fe3+、NO3-、Cl- |
| D、c(NH3?H2O)=1mol?L-1的溶液中:NH4+、Al3+、SO42-、Cl- |
 某有机物M的球棍模型如图所示:
某有机物M的球棍模型如图所示:

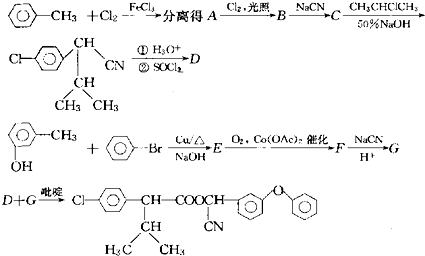
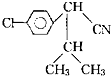
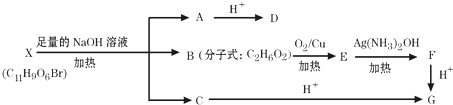
 (其中Ⅰ、Ⅱ为未知部分的结构),为推测X的分子结构,进行如图所示的转化过程:
(其中Ⅰ、Ⅱ为未知部分的结构),为推测X的分子结构,进行如图所示的转化过程: