题目内容
16.下列化学用语正确的是( )| A. | 次氯酸钙的化学式:CaClO | |
| B. | 氟离子结构示意图: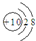 | |
| C. | 质量数为127的钡原子:127Ba | |
| D. | 硫酸的电离方程式:H2SO4═2H+SO${\;}_{4}^{2-}$ |
分析 A.次氯酸钙中阳离子与阴离子个数比为1:2;
B.氟离子的核电荷数为9,核外电子总数为10;
C.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数;
D.硫酸为强电解质,在溶液中完全电离出氢离子和硫酸根离子.
解答 解:A.漂白粉有效成分为次氯酸钙,其正确的化学式为:Ca(ClO)2,故A错误;
B.氟离子的核电荷数为9,氟离子正确的结构示意图为: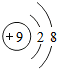 ,故B错误;
,故B错误;
C.钡元素的质子数为56,质量数为127的钡原子可以表示为:56127Ba,故C错误;
D.硫酸为强电解质,硫酸的电离方程式为:H2SO4=2H++SO42-,故D正确;
故选D.
点评 本题考查化学用语的表示方法,为高频考点,题目难度中等,试题基础性强,涉及化学式、离子结构示意图、电离方程式及原子表示方法等,注意掌握常见化学用语的概念及书写原则,试题侧重考查学生的规范答题能力.

练习册系列答案
相关题目
8.Li-Al/FeS电池是一种正在开发的车载电池,该电池正极的反应式为:2Li++FeS+2e-=Li2S+Fe 有关该电池的下列说法中,错误的是( )
| A. | Li-Al在电池中作为负极材料,电极反应式:Li-e-=Li+ | |
| B. | 该电池的电池反应式为:2Li+FeS=Li2S+Fe | |
| C. | 充电时,阴极发生的电极反应式为:Li2S+Fe-2e-═2Li++FeS | |
| D. | 放电时,Li+向正极迁移 |
7.下列说法中错误的是( )
①化学性质相似的有机物是同系物
②分子组成相差一个或几个CH2原子团的有机物是同系物
③若烃中碳、氢元素的质量分数相同,它们必定是同系物
④互为同分异构体的两种有机物的物理性质有差别,但化学性质必定相似
⑤分子式为C3H6与C6H12的两种有机物一定互为同系物
⑥互为同系物的有机物其相对分子质量数值一定相差14n(n为正整数)
①化学性质相似的有机物是同系物
②分子组成相差一个或几个CH2原子团的有机物是同系物
③若烃中碳、氢元素的质量分数相同,它们必定是同系物
④互为同分异构体的两种有机物的物理性质有差别,但化学性质必定相似
⑤分子式为C3H6与C6H12的两种有机物一定互为同系物
⑥互为同系物的有机物其相对分子质量数值一定相差14n(n为正整数)
| A. | 只有①②③④ | B. | 只有①②③④⑤ | C. | 只有②③④ | D. | 只有①②③ |
4. 在温度T1和T2下,X2(g)和H2(g)反应生成HX(g)的平衡常数K如下表:
在温度T1和T2下,X2(g)和H2(g)反应生成HX(g)的平衡常数K如下表:
(1)仅依据K的变化可推断出随着卤素原子核电荷数的增加cd(填字母)
a.HX的还原性逐渐减弱 b.X2与H2反应的剧烈程度逐渐减弱
c.HX的稳定性逐渐减弱 d.在相同条件下,X2的平衡转化率逐渐降低
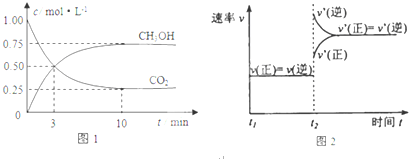
(2)在容积为3L的密闭容器中,由I2(g)和H2(g)合成HI(g),在其他条件不变的情况下,研究温度对反应的影响,HI的物质的量的变化情况如图所示:
①温度为T1时,在0~tAmin内,H2的消耗速率v (H2)=$\frac{{n}_{A}}{6{t}_{A}}$mol/(L•min)
②分析图象,下列说法正确的是a、b(填序号)
a.平衡常数K随温度的升高而变小 b.正反应为放热反应
c.只有当反应进行到A点或B点所示状态时,容器内气体密度才不再发生变化
(3)已知氢氟酸(HF)是弱酸,加水稀释0.1mol•L-1HF溶液,下列各量中增大的是D(填序号)
a.c(H+) b.HF的电离常数 c.c(F-)/c(H+) d.c(H+)/c(HF)
(4)向盛有10滴0.1mol•L-1AgNO3溶液的试管中滴加0.1mol•L-1 NaCl溶液至不再有白色沉淀生成,向其中再滴加0.1mol•L-1KI溶液,出现了黄色沉淀.请简要解释此现象的原因:AgI溶解度比AgCl溶解度小,使AgCl(s)?Ag+(aq)+Cl-(aq)体系中c(Ag+)减小,使平衡向右移动.
 在温度T1和T2下,X2(g)和H2(g)反应生成HX(g)的平衡常数K如下表:
在温度T1和T2下,X2(g)和H2(g)反应生成HX(g)的平衡常数K如下表:| 化学方程式 | K(t1) | K(t2) |
| F2+H2?2HF | 1.8×1036 | 1.9×1032 |
| Cl2+H2?2HCl | 9.7×1012 | 4.2×1011 |
| Br2+H2?2HBr | 5.6×107 | 9.3×106 |
| I2+H2?2HI | 43 | 34 |
a.HX的还原性逐渐减弱 b.X2与H2反应的剧烈程度逐渐减弱
c.HX的稳定性逐渐减弱 d.在相同条件下,X2的平衡转化率逐渐降低
(2)在容积为3L的密闭容器中,由I2(g)和H2(g)合成HI(g),在其他条件不变的情况下,研究温度对反应的影响,HI的物质的量的变化情况如图所示:
①温度为T1时,在0~tAmin内,H2的消耗速率v (H2)=$\frac{{n}_{A}}{6{t}_{A}}$mol/(L•min)
②分析图象,下列说法正确的是a、b(填序号)
a.平衡常数K随温度的升高而变小 b.正反应为放热反应
c.只有当反应进行到A点或B点所示状态时,容器内气体密度才不再发生变化
(3)已知氢氟酸(HF)是弱酸,加水稀释0.1mol•L-1HF溶液,下列各量中增大的是D(填序号)
a.c(H+) b.HF的电离常数 c.c(F-)/c(H+) d.c(H+)/c(HF)
(4)向盛有10滴0.1mol•L-1AgNO3溶液的试管中滴加0.1mol•L-1 NaCl溶液至不再有白色沉淀生成,向其中再滴加0.1mol•L-1KI溶液,出现了黄色沉淀.请简要解释此现象的原因:AgI溶解度比AgCl溶解度小,使AgCl(s)?Ag+(aq)+Cl-(aq)体系中c(Ag+)减小,使平衡向右移动.
11.利用下列装置(部分仪器已省略),能顺利完成对应实验的是( )
| A. | 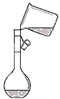 是向容量瓶转移溶液 | |
| B. |  制取氢氧化亚铁 | |
| C. | 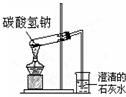 是碳酸氢钠受热分解 | |
| D. | 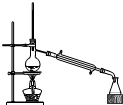 分离四氯化碳(沸点76.75℃)和甲苯(沸点为110.6℃)的混合物 |
1.当不慎有大量Cl2逸到周围空气里时,可用浸有一定浓度的下列物质溶液的毛巾捂住鼻子,该物质是( )
| A. | NaOH | B. | NaCl | C. | NH3•H2O | D. | NaHCO3 |
5.下列有关化学用语表示正确的是( )
| A. | 羟基的电子式: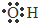 | B. | 聚丙烯的结构简式: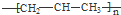 | ||
| C. | 丙烷分子的比例模型为: | D. | 邻羟基苯甲酸的结构简式: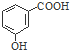 |
6.下列“化学与生活”的说法中,不正确的是( )
| A. | 葡萄糖注射液不能产生丁达尔现象,所以它不属于胶体 | |
| B. | 盐卤可用于制豆腐 | |
| C. | 明矾可用于水的消毒、杀菌 | |
| D. | 碳酸氢钠能用于治疗胃酸过多 |