题目内容
15.A、B、C、D、E为原子序数依次增大的短周期主族元素,A原子的最外层电子数为内层电子数的2倍,B原子的M电子层有1个电子,C的氢氧化物既能与强酸反应又能与强碱反应,D的最高正价和最低负价的代数和为4,E在同周期主族元素中原子半径最小.下列叙述错误的是( )| A. | 元素C位于周期表中第三周期ⅢA族 | |
| B. | 电解熔融化合物CE3可制取单质C | |
| C. | D的最高价含氧酸的浓溶液与单质A共热时能生成三种氧化物 | |
| D. | 化合物B2D2中既含离子键又含非极性共价键 |
分析 A、B、C、D、E为原子序数依次增大的短周期主族元素,A原子的最外层电子数为内层电子数的2倍,则A为C元素;B原子的M电子层有1个电子,则B为Na元素;C的氢氧化物既能与强酸反应又能与强碱反应,C为Al元素;D的最高正价和最低负价的代数和为4,则D为S元素;E在同周期主族元素中原子半径最小,E只能为Cl,以此来解答.
解答 解:由上述分析可知,A、B、C、D、E分别为C、Na、Al、S、Cl,
A.元素C为Al,位于周期表中第三周期ⅢA族,故A正确;
B.CE3为共价化合物,熔融状态不导电,故B错误;
C.D的最高价含氧酸的浓溶液为浓硫酸,与单质A共热时能生成二氧化碳、二氧化硫、水三种氧化物,故C正确;
D.化合物Na2S2中既含离子键又含S-S非极性共价键,类似过氧化钠中化学键,故D正确;
故选B.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子结构、元素的位置和性质推断元素为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案
相关题目
5.下列说法正确的是( )
| A. | 某盐溶液与NaOH溶液共热,产生使湿润红色石蕊试纸变蓝气体,说明原溶液中存在NH4+ | |
| B. | 某溶液中加入硝酸银溶液时,产生白色沉淀,说明原溶液中含有Cl- | |
| C. | 用铂丝蘸取某溶液在酒精灯上灼烧时,火焰呈黄色,说明原溶液中一定含有NaCl | |
| D. | 某溶液中加入BaCl2溶液生成白色沉淀,说明原溶液中有SO42- |
6.化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
| A. | H2S的电子式 | B. | Cl-的结构示意图 | C. | CO2的电子式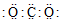 | D. | 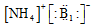 |
3.为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤,②加过量NaOH溶液,③加适量盐酸,④加过量Na2CO3溶液,⑤加过量BaCl2溶液.正确的操作顺序是( )
| A. | ④②⑤③① | B. | ⑤②④①③ | C. | ②⑤④③① | D. | ④①②⑤③ |
10.将固体NH4I置于密闭容器中,在某温度下发生下列反应:
①NH4I(s)?NH3(g)+HI(g)
②2HI(g)?H2(g)+I2(g)
当反应达到平衡时,c(H2)=1mol/,c(HI)=4mol/L,则反应①的化学平衡常数为( )
①NH4I(s)?NH3(g)+HI(g)
②2HI(g)?H2(g)+I2(g)
当反应达到平衡时,c(H2)=1mol/,c(HI)=4mol/L,则反应①的化学平衡常数为( )
| A. | 36 | B. | 24 | C. | 20 | D. | 10 |
20.对羟基扁桃酸是合成农药、香料等的重要中间体,它可由苯酚和乙醛酸在一定条件下反应制得.
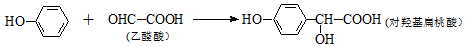
下列有关说法不正确的是( )
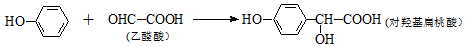
下列有关说法不正确的是( )
| A. | 上述反应的原子利用率可达100% | |
| B. | 上述反应类型为取代反应 | |
| C. | 对羟基扁桃酸可发生加成反应、取代反应和缩聚反应 | |
| D. | 1 mol对羟基扁桃酸与足量NaOH溶液反应,最多可消耗3 mol NaOH |
7.在含有大量的K+、HCO3-、SO42-的溶液中,还可能大量存在的离子是( )
| A. | NH4+ | B. | H+ | C. | OH- | D. | Ba2+ |
4.给定条件下,下列选项中所示的物质间转化均能一步实现的组合是( )
| A. | FeS2$\stackrel{O_{2}/高温}{→}$SO3$\stackrel{H_{2}O}{→}$H2SO4 | |
| B. | HCl(aq)$\stackrel{MnO_{2}}{→}$Cl2$\stackrel{澄清石灰水}{→}$Ca(ClO)2 | |
| C. | N2$→_{△}^{O_{2}/催化剂}$NO2$\stackrel{O_{2}、H_{2}O}{→}$HNO3 | |
| D. | 饱和NaCl溶液$\stackrel{NH_{3}、CO_{2}}{→}$NaHCO3$\stackrel{△}{→}$Na2O3 |
5.一定条件下,在体积为2L的密闭容器中,3molX和3molY发生反应:3X(g)+Y(g)?2Z(g)△H>0,经60s达到平衡,生成0.4molZ.下列说法正确的是( )
| A. | 60s内反应速率为v(X)=0.05mol/(L•s) | |
| B. | 其它条件不变,升高温度,正反应速率增大,逆反应速率减小 | |
| C. | 其它条件不变,若初始投入2mol X和2mol Y则物质Y的转化率减小 | |
| D. | 其它条件不变,将容器体积变为4L,Z的平衡浓度变为原来的一半 |