题目内容
2.用一定量的铁与足量的稀H2SO4 及足量的CuO制取单质铜,有人设计以下两种方案:①Fe$\stackrel{H_{2}SO_{4}}{→}$H2$\stackrel{CuO}{→}$Cu
②CuO$\stackrel{H_{2}SO_{4}}{→}$CuSO4$\stackrel{Fe}{→}$Cu
若按实验原则进行操作,则两者制得单质铜的质量的比较中,正确的是( )
| A. | ①多 | B. | ②多 | C. | 一样多 | D. | 无法判断 |
分析 方案①发生反应:Fe+H2SO4═FeSO4+H2↑、H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O;
方案②发生反应:CuO+H2SO4═CuSO4+H2O、Fe+CuSO4═Cu+FeSO4;
②中均可完全转化,而①中氢气还原CuO,应先通入氢气排出装置中的空气,实验结束应通入氢气到Cu冷却,防止被氧化,氢气不能全部参与还原反应.
解答 解:方案①发生反应:Fe+H2SO4═FeSO4+H2↑、H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O;
方案②发生反应:CuO+H2SO4═CuSO4+H2O、Fe+CuSO4═Cu+FeSO4;
②中均可完全转化,而方案①中氢气还原氧化铜实验,开始时需先通入一部分氢气,排除装置中的空气,实验结束时还要通一会氢气,以防止生成的铜被氧化,如果不考虑先通后停,相同质量的铁生成铜的质量是相同的,但是由于①中部分氢气被浪费,所以导致方案①获得的铜减少,故方案②生成的铜多,
故选B.
点评 本题考查化学方程式计算、化学实验等,属于易错题目,关键是理解掌握氢气还原氧化铜的实际操作.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.下列各组物质相互混合反应后,既有气体生成,最终又有沉淀生成的是( )
①金属钠投入到FeCl3溶液中
②过量Ba(OH)2浓溶液和NH4Al(SO4)2溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中
④Na2O2投入Ca(HCO3)2溶液中.
①金属钠投入到FeCl3溶液中
②过量Ba(OH)2浓溶液和NH4Al(SO4)2溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中
④Na2O2投入Ca(HCO3)2溶液中.
| A. | 只有①④ | B. | 只有③ | C. | 只有②③ | D. | 只有①②④ |
13.固体储氢材料氨硼烷,化学式为NH3BH3,可用如下反应制取:Ni(NH3)6Cl2+2NaBH4=2NH3BH3+4NH3↑+2NaCl+H2↑+Ni.下列说法正确的是( )
| A. | NaBH4中B元素化合价为+3 | B. | 每生成11.2 L氏转移Na个电子 | ||
| C. | NaBH4在反应中作氧化剂 | D. | NH3BH3在反应中属于还原产物 |
10.正确的下列选项的实验操作中是( )
| A. | 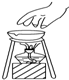 移开加热的蒸发皿 | B. | 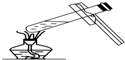 给试管加热 | ||
| C. |  滴加液体 | D. | 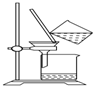 过滤 |
17.已知氧化还原反应:2Cu(IO3)2+24KI+12H2SO4═2CuI↓+13I2+12K2SO4+12H2O,下列说法正确的是( )
| A. | Cu(IO3)2作氧化剂,Cu(IO3)2中的铜和碘元素被还原 | |
| B. | CuI既是氧化产物又是还原产物 | |
| C. | 每生成1 mol CuI,有12 mol KI发生氧化反应 | |
| D. | 每转移1.1 mol电子,有0.2 mol IO3-被氧化 |
7.下列物质的名称错误的是( )
| A. | 2,2-二甲基-3-丁烯 | B. | 2,2-二甲基-3-乙基庚烷 | ||
| C. | 2-甲基-3-乙基戊烷 | D. | 2,3-二甲基戊烷 |
14.下列物质按“赤、橙、黄、绿、蓝、紫”的颜色顺序编排的一组是( )
①溴水 ②CuSO4 ③KMnO4 ④CuO ⑤AgI ⑥FeSO4﹒7H2O⑦CuSO4﹒5H2O
⑧Fe2O3 ⑨Ag2S.
①溴水 ②CuSO4 ③KMnO4 ④CuO ⑤AgI ⑥FeSO4﹒7H2O⑦CuSO4﹒5H2O
⑧Fe2O3 ⑨Ag2S.
| A. | ①②③④⑤⑥ | B. | ③④⑤⑥⑧② | C. | ⑧①⑤⑥⑦③ | D. | ⑧⑨⑤⑥②③ |
11.下列反应的离子方程式正确的是( )
| A. | 石灰石与盐酸反应:CO32-+2H+═H2O+CO2↑ | |
| B. | 石灰乳与Na2CO3溶液混合:Ca(OH)2+CO32-═CaCO3↓+2OH- | |
| C. | 铁与稀硫酸:2Fe+6H+═2Fe3++3 H2↑ | |
| D. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-+H++OH-═BaSO4↓+H2O |
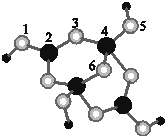 (1)区分晶体和非晶体常用方法为X-射线衍射实验.
(1)区分晶体和非晶体常用方法为X-射线衍射实验.