题目内容
12.下列各组离子能大量共存于同一溶液中,且加入少量NaOH溶液或少量稀硫酸时都能产生白色沉淀的是( )| A. | Ba2+、Mg2+、NO3-、CO32- | B. | Na+、Ag+、Cl-、Ba2+ | ||
| C. | K+、Ba2+、Cl-、HCO3- | D. | Ba2+、Na+、NO3-、Cl- |
分析 根据离子之间不能结合生成沉淀、气体、水等,则离子大量共存,并结合加入少量NaOH溶液或少量稀硫酸时都能产生白色沉淀来解答.
解答 解:A.Ba2+、Mg2+均与CO32-结合生成沉淀,不能大量共存,故A不选;
B.Ag+、Cl-结合生成沉淀,不能大量共存,故B不选;
C.该组离子之间不反应,可大量共存,加入NaOH生成碳酸钡沉淀,加稀硫酸生成硫酸钡沉淀,故C选;
D.该组离子之间不反应,可大量共存,但加入NaOH不生成沉淀,故D不选;
故选C.
点评 本题考查离子的共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应的判断,题目难度不大.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案
相关题目
下列除杂方案错误的是
选项 | 被提纯的物质 | 杂质 | 除杂试剂 | 除杂方法 |
A | CO(g) | CO2(g) | NaOH溶液、浓H2SO4 | 洗气 |
B | NH4Cl(aq) | Fe3+(aq) | NaOH溶液 | 过滤 |
C | Cl2(g) | HCl(g) | 饱和食盐水、浓H2SO4 | 洗气 |
D | Na2CO3(s) | NaHCO3(s) | — | 灼烧 |
3.ClO2是一种消毒杀菌剂,实验室可通过下列反应制得 ClO2:2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O 下列说法正确的是( )
| A. | KClO3在反应中是还原剂 | |
| B. | ClO2是氧化产物 | |
| C. | H2C2O4在反应中被氧化 | |
| D. | 1molKClO3参加反应,有 2mol 电子转移 |
20.在一定温度下的定容容器中,当下列哪些物理量不再发生变化时,表明反应( )
A(s)+2B(g)?C(g)+D(g)已达到平衡状态的是
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度
④混合气体总物质的量 ⑤v(B)正与v(D)逆的比值为2:1 ⑥混合气体总质量.
A(s)+2B(g)?C(g)+D(g)已达到平衡状态的是
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度
④混合气体总物质的量 ⑤v(B)正与v(D)逆的比值为2:1 ⑥混合气体总质量.
| A. | ①③④⑤ | B. | ②③⑤⑥ | C. | ②③④⑤ | D. | ①②③⑥ |
7.水的电离平衡曲线如图所示,下列说法不正确的是( )
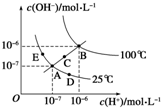

| A. | 图中五点Kw的关系:B>C>A=D=E | |
| B. | 若从A 点到D 点,可采用:温度不变向水中加入少量的酸 | |
| C. | 若从A 点到C 点,可采用:温度不变向水中加入适量的NH4Cl 固体 | |
| D. | 若处在B 点时,将pH=2 的硫酸与pH=10 的KOH 溶液等体积混合后,溶液显中性 |
17.某烃完全燃烧生成CO25.28g和H2O 2.16g,经测定这种烃在标准状况下的密度为3.75g/L,则其分子式是( )
| A. | CH4 | B. | C3H8 | C. | C4H10 | D. | C6H12 |
4.已知同周期X、Y、Z三种元素的最高价氧化物对应水化物酸性由强到弱的顺序为:HXO4>H2YO4>H3ZO4,则下列判断中正确的是( )
| A. | 元素非金属性按X、Y、Z的顺序增强 | |
| B. | 原子半径按X、Y、Z的顺序减小 | |
| C. | 气态氢化物的稳定性按X、Y、Z的顺序增强 | |
| D. | 单质的氧化性按X、Y、Z的顺序减弱 |
1.下列物质属于强电解质的是( )
| A. | 碳酸钙 | B. | 盐酸 | C. | 酒精 | D. | 醋酸 |
