题目内容
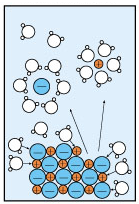
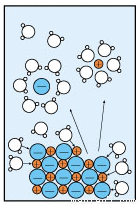
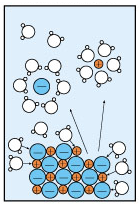 如图为NaCl加入水中溶解并电离的示意图,观察该图可得到的结论是
如图为NaCl加入水中溶解并电离的示意图,观察该图可得到的结论是
- A.该过程通常表示为NaCl=Na++Cl-
- B.NaCl只有在水分子的作用下才能形成Na+
- C.NaCl的水溶液是电解质
- D.NaCl只有在水溶液中才能导电
A
分析:电解质首先必须是化合物,氯化钠是强电解质,在水溶液里或熔融状态下能完全电离,据此分析解答.
解答:A.氯化钠是强电解质,在水溶液里完全电离,所以其电离方程式为NaCl=Na++Cl-,故A正确;
B.氯化钠在水溶液里或熔融状态下都能电离出钠离子,故B错误;
C.氯化钠的水溶液是混合物,所以不是电解质,故C错误;
D.氯化钠是离子化合物,氯化钠在水溶液里或熔融状态下都能电离出阴阳离子,所以氯化钠的水溶液或熔融氯化钠都能导电,故D错误;
故选A.
点评:本题考查电解质电离,注意强电解质和弱电解质电离方程式的区别,为易错点.
分析:电解质首先必须是化合物,氯化钠是强电解质,在水溶液里或熔融状态下能完全电离,据此分析解答.
解答:A.氯化钠是强电解质,在水溶液里完全电离,所以其电离方程式为NaCl=Na++Cl-,故A正确;
B.氯化钠在水溶液里或熔融状态下都能电离出钠离子,故B错误;
C.氯化钠的水溶液是混合物,所以不是电解质,故C错误;
D.氯化钠是离子化合物,氯化钠在水溶液里或熔融状态下都能电离出阴阳离子,所以氯化钠的水溶液或熔融氯化钠都能导电,故D错误;
故选A.
点评:本题考查电解质电离,注意强电解质和弱电解质电离方程式的区别,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
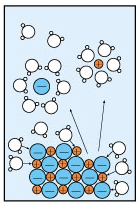 如图为NaCl加入水中溶解并电离的示意图,观察该图可得到的结论是( )
如图为NaCl加入水中溶解并电离的示意图,观察该图可得到的结论是( ) 如图为阳离子交换膜法电解饱和食盐水原理示意图.下列说法不正确的是( )
如图为阳离子交换膜法电解饱和食盐水原理示意图.下列说法不正确的是( )