题目内容
铁和铜是两种重要的金属元素.
(1)铜可溶于稀H2SO4和H2O2混合液中,写出该反应的化学方程式: .
(2)等质量的铁和铜分别与足量的硫粉在加热下充分反应,消耗硫粉的质量比为 (写最简整数比).
(3)向含有KOH和Fe(OH)3的悬浊液中通人氯气,可生成一种水处理剂K2FeO4.反应的化学方程式为 .
(4)铜与浓硫酸反应时会产生难溶性固体甲,其成分可能是CuS、Cu2S或Cu2O,某实验小组设计如下实验对其成分进行探究.
已知:①Cu2O在酸性环境下会发生自身氧化还原反应生成Cu2+和Cu;②CuS和Cu2S均不溶于稀盐酸.
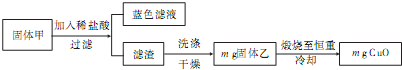
根据实验现象和数据可以确定固体甲中一定含有的成分及其物质的量之比为 ;可能含有的成分是 .
(1)铜可溶于稀H2SO4和H2O2混合液中,写出该反应的化学方程式:
(2)等质量的铁和铜分别与足量的硫粉在加热下充分反应,消耗硫粉的质量比为
(3)向含有KOH和Fe(OH)3的悬浊液中通人氯气,可生成一种水处理剂K2FeO4.反应的化学方程式为
(4)铜与浓硫酸反应时会产生难溶性固体甲,其成分可能是CuS、Cu2S或Cu2O,某实验小组设计如下实验对其成分进行探究.
已知:①Cu2O在酸性环境下会发生自身氧化还原反应生成Cu2+和Cu;②CuS和Cu2S均不溶于稀盐酸.

根据实验现象和数据可以确定固体甲中一定含有的成分及其物质的量之比为
考点:常见金属元素的单质及其化合物的综合应用
专题:
分析:(1)铜可溶于稀H2SO4和H2O2混合液中发生氧化还原反应生成硫酸铜和水;
(2)铁、铜与硫反应的化学方程式分别是:Fe+S
FeS、2Cu+S
Cu2S.据此化学方程式定量关系计算;
(3)向含有KOH和Fe(OH)3的悬浊液中通人氯气,可生成一种水处理剂K2FeO4.根据得失电子守恒、元素守恒即可完成方程式;
(4)首先根据实验现象做判断:由滤液呈蓝色可知,固体甲中一定含有Cu2O,则固体乙中一定含有Cu.煅烧CuS的反应方程式为2CuS+3O2
2CuO+2SO2,该反应固体质量减少;煅烧Cu2S的反应方程式为Cu2S+2O2
2CuO+SO2,该反应是固体质量不变的反应;煅烧Cu时固体质量肯定会增加.由于反应前后固体质量不变,所以固体乙中一定含有Cu和CuS,但是否含有Cu2S无法确定,可假设其有,结合元素守恒列式计算.
(2)铁、铜与硫反应的化学方程式分别是:Fe+S
| ||
| ||
(3)向含有KOH和Fe(OH)3的悬浊液中通人氯气,可生成一种水处理剂K2FeO4.根据得失电子守恒、元素守恒即可完成方程式;
(4)首先根据实验现象做判断:由滤液呈蓝色可知,固体甲中一定含有Cu2O,则固体乙中一定含有Cu.煅烧CuS的反应方程式为2CuS+3O2
| ||
| ||
解答:
解:(1)铜可溶于稀H2SO4和H2O2混合液中发生氧化还原反应,反应的化学方程式为:Cu+H2O2+H2SO4=CuSO4+2H2O,故答案为:Cu+H2O2+H2SO4=CuSO4+2H2O;
(2)铁、铜与硫反应的化学方程式分别是:Fe+S
FeS、2Cu+S
Cu2S.假定铁、铜的质量均为m,可求得消耗S的质量分别为
、
,二者之比为16:7,
故答案为:16:7;
(3)向含有KOH和Fe(OH)3的悬浊液中通人氯气,可生成一种水处理剂K2FeO4.根据得失电子守恒、元素守恒即可完成方程式,10KOH+3Cl2+2Fe(OH)3=2K2FeO4+6KCl+8H2O;
故答案为:10KOH+3Cl2+2Fe(OH)3=2K2FeO4+6KCl+8H2O;
(4)首先根据实验现象做判断:由滤液呈蓝色可知,固体甲中一定含有Cu2O,则固体乙中一定含有Cu.煅烧CuS的反应方程式为2CuS+3O2
2CuO+2SO2,该反应固体质量减少;煅烧Cu2S的反应方程式为Cu2S+2O2
2CuO+SO2,该反应是固体质量不变的反应;煅烧Cu时固体质量肯定会增加.由于反应前后固体质量不变,所以固体乙中一定含有Cu和CuS,但是否含有Cu2S无法确定,可假设其有.设固体甲中Cu2O、CuS、Cu2S的物质的量分别为xmol、ymol、zmol,则固体乙中含有Cu、CuS、Cu2S的物质的量分别为0.5xmol、ymol、zmol,即:32x+96y+160z=m;根据铜元素守恒可得:80(0.5x+y+2z)=m.两式联立得:x=2y,即Cu2O、CuS的物质的量之比为2:1;
故答案为:2:1; Cu2S.
(2)铁、铜与硫反应的化学方程式分别是:Fe+S
| ||
| ||
| 32m |
| 56 |
| 32m |
| 128 |
故答案为:16:7;
(3)向含有KOH和Fe(OH)3的悬浊液中通人氯气,可生成一种水处理剂K2FeO4.根据得失电子守恒、元素守恒即可完成方程式,10KOH+3Cl2+2Fe(OH)3=2K2FeO4+6KCl+8H2O;
故答案为:10KOH+3Cl2+2Fe(OH)3=2K2FeO4+6KCl+8H2O;
(4)首先根据实验现象做判断:由滤液呈蓝色可知,固体甲中一定含有Cu2O,则固体乙中一定含有Cu.煅烧CuS的反应方程式为2CuS+3O2
| ||
| ||
故答案为:2:1; Cu2S.
点评:本题考查了元素化合物性质的分析判断,氧化还原反应的分析判断,化学方程式的定量计算应用,掌握基础是关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
巴豆酸的结构简式为CH3-CH=CH-COOH.现有①氯化氢;②溴水;③纯碱溶液;④丁醇;⑤酸性高锰酸钾溶液.试根据巴豆酸的结构特点,判断在一定条件下,能与巴豆酸反应的物质是( )
| A、②④⑤ | B、①③④ |
| C、①②③④ | D、①②③④⑤ |
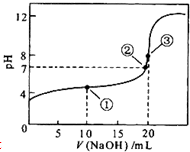 常温下,用0.1mol?L-1 NaOH溶液滴定20mL 0.1mol?L-1CH3COOH溶液的滴定曲线如图所示.下列说法正确的是( )
常温下,用0.1mol?L-1 NaOH溶液滴定20mL 0.1mol?L-1CH3COOH溶液的滴定曲线如图所示.下列说法正确的是( )| A、点①所示溶液中:c(Na+)>c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-) | ||
| B、点②所示溶液中:c(Na+)+c(H+)=c(CH3COO-)+c(CH3COOH)+c(OH-) | ||
| C、点③所示溶液中:c(CH3COO-)>c(Na+)>c(OH-)>c(H+) | ||
D、在整个滴定过程中:溶液中
|
芳块类大环化合物是新兴的一种富碳共轭大环状分子.苯乙炔( 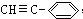 )可用合成一系列芳炔类大环化合物,其结构如下,有关叙述正确的是( )
)可用合成一系列芳炔类大环化合物,其结构如下,有关叙述正确的是( )
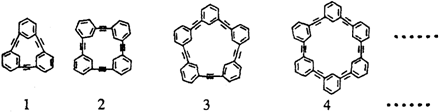
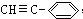 )可用合成一系列芳炔类大环化合物,其结构如下,有关叙述正确的是( )
)可用合成一系列芳炔类大环化合物,其结构如下,有关叙述正确的是( )
| A、上述四种物质属于苯乙炔的同系物 |
| B、第一种物质的分子式为C18H12 |
| C、它们可通过苯乙炔的加成反应获得 |
| D、该系列化合物的含碳量均相同 |



