题目内容
15.一定温度下,将 3mol SO2 和 1mol O2 充入一定容密闭容器中,在催化剂存 在下进行下列反应:2SO2(g)+O2(g)?2SO3(g);当达到平衡状态时,下列说法中正确的是( )| A. | 生成 SO3 为 2 mol | |
| B. | SO2 和 SO3 物质的量之和一定为 3 mol | |
| C. | 1molO2 恰好反应完 | |
| D. | SO2 的物质的量和 SO3 物质的量一定相等 |
分析 A.可逆反应的特点:反应不能进行到底.可逆反应无论进行多长时间,反应物都不可能100%地全部转化为生成物;
B.根据元素守恒进行判断;
C.可逆反应的特点:反应不能进行到底.可逆反应无论进行多长时间,反应物都不可能100%地全部转化为生成物;
D.SO2的物质的量和SO3物质的量的大小关系取决于原始投料量和转化率.
解答 解:A.可逆反应无论进行多长时间,反应物都不可能100%地全部转化为生成物,故生成SO3小于2mol,故A错误;
B.根据S元素守恒可知,S的总的物质的量保持不变,即SO2和SO3物质的量之和一定为3mol,故B正确;
C.可逆反应无论进行多长时间,反应物都不可能100%地全部转化为生成物,故1molO2 不可能反应完,故C错误;
D.SO2的物质的量和SO3物质的量的大小关系取决于原始投料量和转化率,故D错误,
故选B.
点评 本题考查可逆反应的特点,难度不大,要注意可逆反应无论进行多长时间,反应物都不可能100%地全部转化为生成物.

练习册系列答案
相关题目
8.用酸性氢氧燃料电池为电源进行电解的实验装置示意图如图所示.下列说法中,正确的是( )
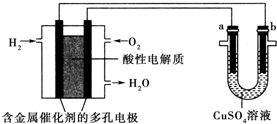

| A. | 燃料电池工作时,正极反应为O2+2H2O+4e-═4OH- | |
| B. | 此装置用于铁表面镀铜时,a为铁 | |
| C. | a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 | |
| D. | a、b两极均是石墨时,在相同条件下,a极产生的气体与电池中消耗的H2体积相等 |
10.下列说法正确的是( )
| A. | 只含一种分子的物质是纯净物,只含一种元素的物质也是纯净物 | |
| B. | 医疗上的血液透析利用了胶体的性质 | |
| C. | NH3溶于水后所得的溶液可以导电,所以NH3为电解质 | |
| D. | 从海水中可以得到NaCl,电解NaCl溶液可制备Na |
20.某原电池构造如图所示.下列有关叙述正确的是( )

| A. | 在外电路中,电子由银电极流向铜电极 | |
| B. | 取出盐桥后,电流计的指针仍发生偏转 | |
| C. | 外电路中每通过0.1 mol电子,铜的质量理论上减小6.4 g | |
| D. | 原电池的总反应式为Cu+2AgNO3=2Ag+Cu(NO3)2 |
4.下列叙述正确的是( )
| A. | 既能与酸又能与碱反应的物质一定是两性氧化物或两性氢氧化物 | |
| B. | 往Fe(OH)3胶体中逐滴加入稀H2SO4溶液时,开始时会出现沉淀,再继续滴加时,沉淀又会消失 | |
| C. | 胶体区别于其他分散系的本质特征是丁达尔现象 | |
| D. | 某物质溶于水后所得溶液能导电,该物质一定属于电解质 |
5.有机物M是合成某药品的中间体,结构简式如图所示.下列说法错误的是( )
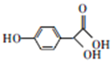

| A. | 用钠可检验M分子中存在羟基 | B. | M能发生酯化、加成、氧化反应 | ||
| C. | M的分子式为C8H8O4 | D. | M的苯环上一硝基代物有2种 |
