题目内容
12.下列实验方案中,不能达到实验目的是( )| 项目 | 实验目的 | 实验方案 |
| A | 验证稀硫酸和稀硝酸的氧化性强弱 | 将两块相同的铜片分别加入浓度均为2mol/L的硫酸和硝酸中,观察反应的难易程度 |
| B | 验证Cu、Fe的还原性强弱 | 将铁丝和铜丝分别插入浓硝酸中,观察反应的剧烈程度 |
| C | 验证Br、I非金属性强弱 | 将少量溴水加入KI-淀粉溶液中,观察溶液是否变蓝色 |
| D | 验证Mg、Al的金属性强弱 | 在Mg(OH)2、Al(OH)3中分别加入稀氨水,观察沉淀能否溶解 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.稀硫酸和铜不反应,稀硝酸和铜发生氧化还原反应;
B.常温下铁在浓硝酸中钝化不能继续反应;
C.溴单质氧化性大于碘单质,溴单质氧化碘离子生成碘单质,遇到淀粉变蓝色;
D.金属最高价氧化物对应水化物为碱,碱性越强对应金属的金属性越强,氢氧化镁、氢氧化铝不溶于氨水.
解答 解:A.稀硫酸和铜不反应,稀硝酸和铜发生氧化还原反应,将两块相同的铜片分别加入浓度均为2mol/L的硫酸和硝酸中,观察反应的难易程度,可以比较验证稀硫酸和稀硝酸的氧化性强弱,故A正确;
B.常温下铁在浓硝酸中钝化不能继续反应,将铁丝和铜丝分别插入浓硝酸中,观察反应的剧烈程度不能验证Cu、Fe的还原性强弱,故B错误;
C.溴单质氧化性大于碘单质,溴单质氧化碘离子生成碘单质,遇到淀粉变蓝色,将少量溴水加入KI-淀粉溶液中,观察溶液是否变蓝色可以验证Br、I非金属性强弱,故C正确;
D.金属最高价氧化物对应水化物为碱,碱性越强对应金属的金属性越强,在Mg(OH)2、Al(OH)3中分别加入稀氨水,沉淀都不溶解,不能验证Mg、Al的金属性强弱,故D错误;
故选BD.
点评 本题考查了化学实验方案的设计原理和反应现象的分析,主要是特殊性质的理解应用,掌握基础是解题关键,题目难度中等.

练习册系列答案
相关题目
2.将足量SO2通入下列溶液中,能产生浑浊的有( )
①Ba(OH)2溶液②CaCl2溶液 ③H2S溶液 ④Ba(NO3)2溶液 ⑤Na2SiO3溶液.
①Ba(OH)2溶液②CaCl2溶液 ③H2S溶液 ④Ba(NO3)2溶液 ⑤Na2SiO3溶液.
| A. | ③④⑤ | B. | ②③⑤ | C. | ①③④⑤ | D. | ②③④⑤ |
3.某有机物的结构简式为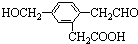 ,它在一定条件下可能发生的反应有( )
,它在一定条件下可能发生的反应有( )
①加成 ②水解 ③取代 ④氧化 ⑤还原 ⑥消去.
 ,它在一定条件下可能发生的反应有( )
,它在一定条件下可能发生的反应有( )①加成 ②水解 ③取代 ④氧化 ⑤还原 ⑥消去.
| A. | ②③④ | B. | ①③⑤⑥ | C. | ①③④⑤ | D. | ①③④⑤⑥ |
20.NA为阿伏加罗常数的值,下列说法正确的是( )
| A. | 1.0L1.0mol•L-1的NaAlO2水溶液中含有的氧原子数为2NA | |
| B. | 常温下,0.1mol碳酸钠晶体中含有CO32-的个数为0.1NA | |
| C. | 标准状况下,11.2L18O2中所含中子数为8NA | |
| D. | 25℃时,1LpH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA |
17.现有甲乙丙丁四种物质,分别由2种或3种元素组成,它们的分子都具有与氩(Ar)相同的电子数.其中乙与NaOH液反应可生成两种盐,两种盐的水溶液均显碱性.下列推断合理的是( )
| A. | 乙可能由3种元素组成 | |
| B. | 若甲与乙中各元素质量比相同,则甲中一定含有氧元素 | |
| C. | 丙中一种元素原子的最外层电子数是内层电子总数的2倍,则丙一定是甲烷的同系物 | |
| D. | 若丁中为双原子分子,则丁中含有的化学键一定是极性键 |
4.下列关于乙烯说法正确的是( )
| A. | 乙烯使酸性高锰酸钾溶液及溴的四氯化碳溶液褪色原理相同 | |
| B. | 工业利用乙烯水化法制乙醇,是发生了取代反应 | |
| C. | 水果运输中为延长果实的成熟期,常在车厢里放置浸泡过高锰酸钾溶液的硅藻土 | |
| D. | 乙烯在空气中燃烧,发生火焰明亮并带有浓烟的火焰 |
1.下列物质与硝酸反应,既体现了硝酸具有强氧化性又体现了酸性的是( )
| A. | Cu | B. | C | C. | CuO | D. | CuCO3 |
2.同周期的两种主族元素A和B能够形成离子化合物AmBn,已知A的原子序数为a,则B的原子序数可能为( )
| A. | a+8+m-n | B. | a+16-m+n | C. | a+24-m-n | D. | a+18-m-n |
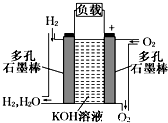 被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点.如图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题:
被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点.如图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题: