题目内容
3.对于下列事实的解释正确的是( )| A. | 氢氟酸可用于雕刻玻璃,说明氢氟酸具有强酸性 | |
| B. | 浓硝酸在光照下颜色变黄,说明浓硝酸具有强氧化性 | |
| C. | 常温下浓硫酸可用铝罐贮存,说明铝与浓硫酸不反应 | |
| D. | 氨水可使酚酞试剂变为红色,说明氨水显碱性 |
分析 A.HF酸为弱酸,能与二氧化硅反应;
B.浓硝酸光照分解;
C.常温下浓硫酸与铝发生钝化,生成致密的氧化膜阻止反应进一步发生;
D.一水合氨电离出氢氧根离子.
解答 解:A.HF酸为弱酸,但能与二氧化硅反应,则氢氟酸可用于雕刻玻璃,故A错误;
B.浓硝酸光照分解生成的二氧化氮溶解在溶液中为黄色,与硝酸的强氧化性无关,故B错误;
C.常温下浓硫酸与铝发生钝化,生成致密的氧化膜阻止反应进一步发生,则常温下浓硫酸可用铝罐贮存,故C错误;
D.一水合氨电离出氢氧根离子,溶液显碱性,则氨水可使酚酞试剂变为红色,故D正确;
故选D.
点评 本题考查元素化合物的性质,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意反应与现象的分析,题目难度不大.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
13.A、B、C、D、E五种短周期主族元素原子序数逐渐增大,其中A与C、B与E分别为同族元素.原子半径A<B<E<D<C,B原子最外层电子数是次外层的3倍,C、D的核外电子数之和与B、E核外电子数之和相等.下列说法正确的是( )
| A. | 简单离子半径:E<D | |
| B. | 气态氢化物的稳定性:B<E | |
| C. | 最高价氧化物对应水化物的碱性:C>D | |
| D. | A与E形成的化合物为离子化合物 |
8.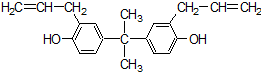 据《华盛顿邮报》报道,美国食品与药物管理局2010年2月公布了一份草拟的评估报告,指出塑料奶瓶和婴儿奶粉罐普遍存在的化学物质双酚A(如图),并不会对婴儿或成人的健康构成威胁.关于双酚A的下列说法正确的是( )
据《华盛顿邮报》报道,美国食品与药物管理局2010年2月公布了一份草拟的评估报告,指出塑料奶瓶和婴儿奶粉罐普遍存在的化学物质双酚A(如图),并不会对婴儿或成人的健康构成威胁.关于双酚A的下列说法正确的是( )
 据《华盛顿邮报》报道,美国食品与药物管理局2010年2月公布了一份草拟的评估报告,指出塑料奶瓶和婴儿奶粉罐普遍存在的化学物质双酚A(如图),并不会对婴儿或成人的健康构成威胁.关于双酚A的下列说法正确的是( )
据《华盛顿邮报》报道,美国食品与药物管理局2010年2月公布了一份草拟的评估报告,指出塑料奶瓶和婴儿奶粉罐普遍存在的化学物质双酚A(如图),并不会对婴儿或成人的健康构成威胁.关于双酚A的下列说法正确的是( )| A. | 该化合物属于芳香烃 | |
| B. | 该化合物分子式为C21H24O2 | |
| C. | 双酚A能使溴水褪色,但不能使酸性高锰酸钾溶液褪色 | |
| D. | 1mol双酚A最多可与4mol浓溴水发生取代反应 |
15.下列说法中错误的是( )
| A. | 乙烷和乙烯的熔点都比CH4的高 | B. | 乙烷和乙烯都可发生加成反应 | ||
| C. | 乙烷能发生氧化反应 | D. | 苯和乙烯都是常见化工原料 |
12.元素性质呈周期性变化的决定因素是( )
| A. | 元素原子半径大小呈周期性变化 | |
| B. | 元素原子量依次递增 | |
| C. | 元素原子核外电子排布呈周期性变化 | |
| D. | 元素的最高正化合价呈周期性变化 |
13.以下转化能通过一步反应实现的是( )
| A. | Al2O3→Al(OH)3 | B. | Al→Na[Al (OH)4] | C. | Fe→Fe(OH)2 | D. | SiO2→H2SiO3 |
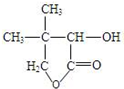 G的合成线路如图:
G的合成线路如图: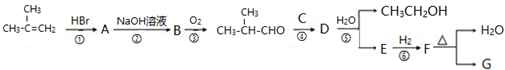
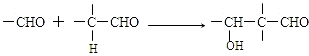
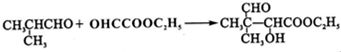 .
. X、Y、Z、W四种短周期元素在周期表中的位置关系如图:若Z元素原子的最外层电子数是电子层数的2倍.
X、Y、Z、W四种短周期元素在周期表中的位置关系如图:若Z元素原子的最外层电子数是电子层数的2倍. .
.