题目内容
氢气燃烧生成液态水的热化学方程式是2H2(g)+O2(g)═2H2O(l);△H=-572kJ/mol 请回答下列问题:
(1)生成物能量总和 (填“大于”、“小于”或“等于”)反应物能量总和.
(2)若2mol氢气完全燃烧生成水蒸气,则放出的热量 (填“>”、“<”或“=”)572kJ.
(3)已知可逆反应N2+3H2?2NH3,每生成2mol的NH3放出热量92kJ,现容器中有6mol H2,2mol N2充分参与反应,不考虑热散失,则放出热量 (填“>”、“<”或“=”)184kJ.
(1)生成物能量总和
(2)若2mol氢气完全燃烧生成水蒸气,则放出的热量
(3)已知可逆反应N2+3H2?2NH3,每生成2mol的NH3放出热量92kJ,现容器中有6mol H2,2mol N2充分参与反应,不考虑热散失,则放出热量
考点:反应热和焓变
专题:化学反应中的能量变化
分析:(1)根据放热反应中生成物能量总和与反应物能量总和的关系;
(2)根据热化学方程式2H2(g)+O2(g)═2H2O(l)△H=-572kJ/mol进行计算以及液态水变成水蒸气需要吸热来判断;
(2)根据热化学方程式2H2(g)+O2(g)═2H2O(l)△H=-572kJ/mol进行计算以及液态水变成水蒸气需要吸热来判断;
解答:
解:(1)因放热反应中生成物能量总<与反应物能量总和,而2H2(g)+O2(g)═2H2O(l)△H=-572kJ/mol是放热反应,故答案为:小于;
(2)据热化学方程式2H2(g)+O2(g)═2H2O(l)△H=-572kJ/mol,2mol氢气完全燃烧生成液态水放出热量572kJ,因液态水变成水蒸气需要吸热,所以2mol氢气完全燃烧生成水蒸气放出热量小于572kJ,故答案为:<.
(3)反应是可逆反应,反应物不能完全转化,6mol H2,2mol N2充分参与反应也不可能生成4molNH3,故放出的热量小于184KJ的热量.
故答案为:<.
(2)据热化学方程式2H2(g)+O2(g)═2H2O(l)△H=-572kJ/mol,2mol氢气完全燃烧生成液态水放出热量572kJ,因液态水变成水蒸气需要吸热,所以2mol氢气完全燃烧生成水蒸气放出热量小于572kJ,故答案为:<.
(3)反应是可逆反应,反应物不能完全转化,6mol H2,2mol N2充分参与反应也不可能生成4molNH3,故放出的热量小于184KJ的热量.
故答案为:<.
点评:本题考查学生能量转化的形式,以及可逆反应的特点,可以根据所学内容来回答,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
若1mol某烷烃燃烧后,测得产物中含有m mol CO2和n mol CO,则该烷烃分子中氢原子个数为( )
| A、m+n |
| B、2(m+n) |
| C、m-n+2 |
| D、2(n+m+1) |
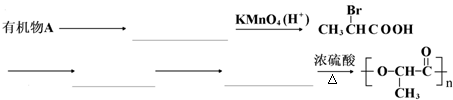
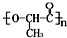 是一种很有前途的可降解高分子材料,可制成袋子替代日常生活中的大部分塑料袋.请完成以有机物A为原料合成聚乳酸的路线(无机试剂任选)
是一种很有前途的可降解高分子材料,可制成袋子替代日常生活中的大部分塑料袋.请完成以有机物A为原料合成聚乳酸的路线(无机试剂任选)