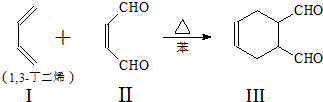
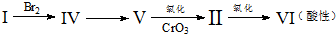题目内容
一定条件下,卤代烃和金属钠能发生伍兹反应:RX+2Na+RX→R-R+2NaX,反应中有C-X键的断裂和C-C键的形成.据此,以下卤代烃伍兹反应的可能产物(不考虑NaX)及命名合理的是( )
| A、一氯甲烷和2-氯丙烷:正丁烷 |
| B、2,2-二甲基-1-氯丙烷与一氯甲烷:3,3-二甲基丁烷 |
| C、1,5-二氯戊烷:环戊烷 |
| D、四氯化碳:金刚石 |
考点:有机物的合成
专题:有机化合物的获得与应用
分析:认真分析反应原理得出:此反应为加长碳链的反应,利用的反应类型为取代反应,即卤代烃中的卤素原子被烃基取代,据此逐一分析各个选项,选择正确答案即可.
解答:
解:A、一氯甲烷和2-氯丙烷反应生成2-甲基丙烷,故A错误;
B、2,2-二甲基-1-氯丙烷与一氯甲烷反应生成:2,2-二甲基丁烷,故B错误;
C、1,5-二氯戊烷自身发生取代反应成环,命名为:环戊烷,故C正确;
D、四氯化碳本身若发生伍兹反应,生成金刚石,故D正确,故选CD.
B、2,2-二甲基-1-氯丙烷与一氯甲烷反应生成:2,2-二甲基丁烷,故B错误;
C、1,5-二氯戊烷自身发生取代反应成环,命名为:环戊烷,故C正确;
D、四氯化碳本身若发生伍兹反应,生成金刚石,故D正确,故选CD.
点评:本题主要考查的是氯代烃的取代反应,熟练掌握所给信息,利用信息判断是解决本题的关键,有一定难度.

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
下列烷烃的沸点是:甲烷:-162℃;乙烷:-89℃;丁烷:-1℃;戊烷:36℃.根据以上数字推断丙烷的沸点可能是( )
| A、约-40℃ |
| B、约-182℃ |
| C、约-108℃ |
| D、约56℃ |
下列有关电化学中的化学用语,说法正确的是( )
| A、用惰性电极电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-═Cl2↑ |
| B、氢氧燃料电池的负极反应式:O2+2H2O+4e-═4OH- |
| C、粗铜精炼时,与电源正极相连的是纯铜,正极反应式为:Cu2++2e-═Cu |
| D、钢铁发生电化学腐蚀的正极反应式:Fe═Fe2++2e- |
有关下列溶液的叙述不正确的是( )
| A、C H3COOH与CH3COONa的混合溶液中:c(CH3COO-)+c(OH-)=c(Na+)+c(H+) |
| B、常温下,0.1mol.L-1CH3COONa溶液和0.1mol.L-1NaHCO3溶液,NaHCO3溶液的pH大 |
| C、0.1mol.L-1的(NH4)2SO4溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
| D、将l mol KC1、l mol KHS溶于水配成的混合溶液中:n(K+)=n(S2-)+n(HS-)+n(H2S) |
常温下,对于下列电解质溶液的说法正确的是( )
| A、pH=1的溶液中,Fe3+、I-、NO3-、K+可以大量共存 |
| B、用过量的NaOH溶液吸收SO2的离子方程式:SO2+OH-=HSO3- |
| C、在c(SO32-)=0.1 mol.L-1的溶液中,Na+、C1-、H+、Ca2+可以大量共存 |
| D、向澄清石灰水中通入氯气,反应的离子方程式:2OH-+Cl2=C1-+C1O-+H2O |
两名日本科学家与一名美国科学家利用钯作催化剂,将有机物进行“裁剪”、“缝合”,创造出具有特殊功能的新物质而获2010年诺贝尔化学奖.下列说法正确的是( )
| A、有机物中一定含有碳和氢两种元素 |
| B、一定条件下,催化剂能提高反应物的转化率 |
| C、将有机物进行“缝合”可以不遵循原子守恒定律 |
| D、将有机物进行“裁剪”需要破坏旧的化学键 |
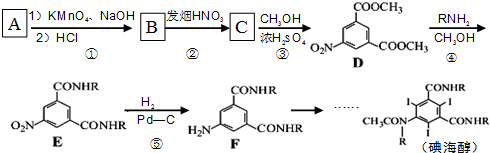
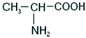 属于α-氨基酸);
属于α-氨基酸);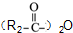 →
→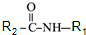 +R2COOH
+R2COOH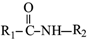 +NaOH→R1COONa+R2NH2
+NaOH→R1COONa+R2NH2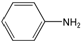 呈弱碱性,易被氧化
呈弱碱性,易被氧化 和(CH3CO)2O为原料制备染料中间体
和(CH3CO)2O为原料制备染料中间体 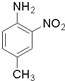 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).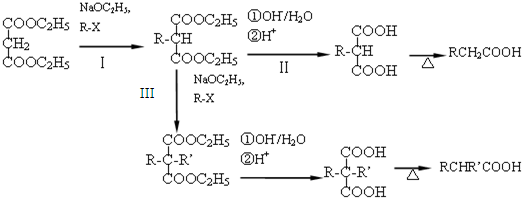
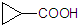 ,所需溴代烃的结构简式为
,所需溴代烃的结构简式为