题目内容
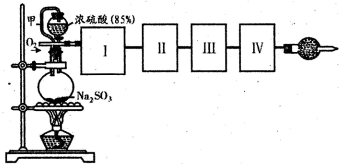
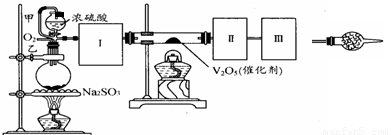
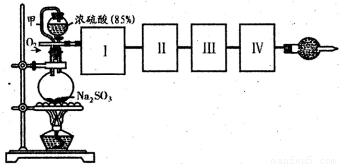
测定转化成SO3的转化率可以用如图装置,装置中烧瓶内发生的化学反应方程式为:
Na2SO3(s)+H2SO4(85%)=Na2SO4+H2O+SO2↑(已知S03的熔点是16.8℃,沸点是44.8℃)

(1)装置中甲管的作用是______.
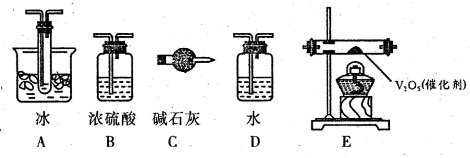
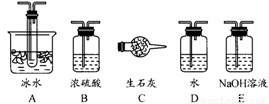
(2)根据实验需要,应该在I、II、III、IV处连接合适的装置,请从题图A?E装置中选择最适合装置并将其序号填放下面的空格中.I、II、III、IV处连接的装置分别是______

(3)为使SO2有较高的转化率,实验中加热催化剂与滴加浓硫酸的顺序中,应采取的操作是______,若用大火加热烧瓶时,SO2的转化率会______ (填“升高”、“不变”或“降低”).
(4)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象不明显,但又不存在气密性问题,请你推测可能的原因(可以不填满)①原因:______②原因:______ ③原因:______
(5)将SO2通入含1mol氯酸的溶液中,可生成一种强酸和一种氧化物,并有6.02×1023个电子转移,则该反应的化学方程式为______
(6)用nmolNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2-段时间后,测得装置IV增重了 mg,则实验中SO2的转化率为______.(用含m、n的代数式填写)
解:(1)由图可知,液体流下时使分液漏斗中压强减小,不利于液体流下,而甲装置能保证分液漏斗和烧瓶内气体压强相等,则甲能使液体顺利流下,故答案为:让硫酸顺利滴下;
(2)因从溶液中反应生成气体中混有水蒸气,则I处应选择B装置来吸收水进行气体的干燥,II中选E进行二氧化硫气体的催化氧化,S03的熔点是16.8℃,沸点是44.8℃,III中选A进行冷却,使三氧化硫与二氧化硫分离,在IV中选择C装置来吸收未反应的SO2,故答案为:BEAC;
(3)因催化剂在一定的温度下催化效果好,则应先加热催化剂,大火加热时反应速率过快,生成的部分二氧化硫未反应就通过了E装置,导致SO2的转化率降低,
故答案为:先加热催化剂再滴入浓硫酸;降低;
(4)SO2气体产生缓慢,可能为Na2SO3变质生成硫酸钠,也可能为浓硫酸的浓度不够,反应速率变慢,故答案为:Na2SO3变质;浓硫酸的浓度不够;
(5)SO2通入含1mol氯酸的溶液中,可生成一种强酸和一种氧化物,有6.02×1023个电子转移,则Cl元素的化合价由+5价降低为+4价,由质量守恒定律可知反应的化学方程式为
SO2+2HClO3═H2SO4+2ClO2,故答案为:SO2+2HClO3═H2SO4+2ClO2;
(6)IV增重了mg,为未反应的SO2的质量,其物质的量为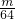 mol,nmolNa2SO3粉末与足量浓硫酸反应生成nmolSO2,则转化率为
mol,nmolNa2SO3粉末与足量浓硫酸反应生成nmolSO2,则转化率为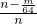 ×100%=
×100%=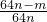 ×100%,
×100%,
故答案为: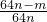 ×100%.
×100%.
分析:(1)根据压强来分析甲的作用;
(2)从除杂、催化氧化、冷却、吸收未反应的SO2,排除空气中水及二氧化碳的影响来分析;
(3)根据催化剂在一定的温度下催化效果好及反应速率来分析;
(4)SO2气体产生缓慢,根据发生的化学反应及影响反应速率的因素来分析;
(5)SO2通入含1mol氯酸的溶液中,可生成一种强酸和一种氧化物,有6.02×1023个电子转移,则Cl元素的化合价由+5价降低为+4价,并利用质量守恒定律来书写反应方程式;
(6)IV增重了mg,为未反应的SO2的质量,nmolNa2SO3粉末与足量浓硫酸反应生成nmolSO2,以此来计算转化率.
点评:本题考查二氧化硫气体的制取及二氧化硫的催化氧化实验,明确装置及装置的作用是解答本题的关键,难度不大,并注意利用守恒法来分析问题.
(2)因从溶液中反应生成气体中混有水蒸气,则I处应选择B装置来吸收水进行气体的干燥,II中选E进行二氧化硫气体的催化氧化,S03的熔点是16.8℃,沸点是44.8℃,III中选A进行冷却,使三氧化硫与二氧化硫分离,在IV中选择C装置来吸收未反应的SO2,故答案为:BEAC;
(3)因催化剂在一定的温度下催化效果好,则应先加热催化剂,大火加热时反应速率过快,生成的部分二氧化硫未反应就通过了E装置,导致SO2的转化率降低,
故答案为:先加热催化剂再滴入浓硫酸;降低;
(4)SO2气体产生缓慢,可能为Na2SO3变质生成硫酸钠,也可能为浓硫酸的浓度不够,反应速率变慢,故答案为:Na2SO3变质;浓硫酸的浓度不够;
(5)SO2通入含1mol氯酸的溶液中,可生成一种强酸和一种氧化物,有6.02×1023个电子转移,则Cl元素的化合价由+5价降低为+4价,由质量守恒定律可知反应的化学方程式为
SO2+2HClO3═H2SO4+2ClO2,故答案为:SO2+2HClO3═H2SO4+2ClO2;
(6)IV增重了mg,为未反应的SO2的质量,其物质的量为
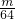 mol,nmolNa2SO3粉末与足量浓硫酸反应生成nmolSO2,则转化率为
mol,nmolNa2SO3粉末与足量浓硫酸反应生成nmolSO2,则转化率为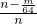 ×100%=
×100%=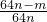 ×100%,
×100%,故答案为:
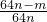 ×100%.
×100%.分析:(1)根据压强来分析甲的作用;
(2)从除杂、催化氧化、冷却、吸收未反应的SO2,排除空气中水及二氧化碳的影响来分析;
(3)根据催化剂在一定的温度下催化效果好及反应速率来分析;
(4)SO2气体产生缓慢,根据发生的化学反应及影响反应速率的因素来分析;
(5)SO2通入含1mol氯酸的溶液中,可生成一种强酸和一种氧化物,有6.02×1023个电子转移,则Cl元素的化合价由+5价降低为+4价,并利用质量守恒定律来书写反应方程式;
(6)IV增重了mg,为未反应的SO2的质量,nmolNa2SO3粉末与足量浓硫酸反应生成nmolSO2,以此来计算转化率.
点评:本题考查二氧化硫气体的制取及二氧化硫的催化氧化实验,明确装置及装置的作用是解答本题的关键,难度不大,并注意利用守恒法来分析问题.

练习册系列答案
相关题目
 Na2SO4+SO2↑+H2O(注:80%H2SO4具有浓硫酸的特性)
Na2SO4+SO2↑+H2O(注:80%H2SO4具有浓硫酸的特性)