题目内容
在酸性介质中,往MnSO4溶液里滴加(NH4)2S2O8溶液会发生如下离子反应(未配平):Mn2++S2O82-+H2O→MnO4-+SO42-+H+,下列说法不正确的是( )
| A、氧化性比较:S2O82->MnO4- |
| B、氧化剂S2O82-的摩尔质量为192g/mol |
| C、该反应中酸性介质可以为盐酸 |
| D、若有0.1mol氧化产物生成,则转移电子0.5mol |
考点:氧化还原反应
专题:
分析:A.氧化还原反应中氧化剂氧化性大于氧化产物的氧化性;
B.根据相对分子质量判断;
C.盐酸为强还原性酸,能被过二硫酸根离子氧化;
D.根据氧化产物和转移电子之间的关系式计算转移电子数.
B.根据相对分子质量判断;
C.盐酸为强还原性酸,能被过二硫酸根离子氧化;
D.根据氧化产物和转移电子之间的关系式计算转移电子数.
解答:
解:A.该反应中,过二硫酸根离子得电子化合价降低为氧化剂,锰离子失电子化合价升高为还原剂,则高锰酸根离子为氧化产物,氧化剂的氧化性大于氧化产物的氧化性,所以氧化性比较:S2O82->MnO4-,故A正确;
B.S2O82-的相对分子质量为2×32+8×16=192,则氧化剂S2O82-的摩尔质量为192g/mol,故B正确;
C.盐酸为强还原性酸,能被过二硫酸根离子氧化生成氯气,所以不能用盐酸作酸性介质,故C错误;
D.若有0.1mol氧化产物MnO4-生成,Mn元素化合价由+2价升高到+7价,则转移电子0.5mol,故D正确.
故选C.
B.S2O82-的相对分子质量为2×32+8×16=192,则氧化剂S2O82-的摩尔质量为192g/mol,故B正确;
C.盐酸为强还原性酸,能被过二硫酸根离子氧化生成氯气,所以不能用盐酸作酸性介质,故C错误;
D.若有0.1mol氧化产物MnO4-生成,Mn元素化合价由+2价升高到+7价,则转移电子0.5mol,故D正确.
故选C.
点评:本题考查了氧化还原反应,为高频考点,侧重于学生的分析能力和计算能力的考查,明确元素化合价是解本题的关键,注意盐酸是强酸且是强还原性酸,易被强氧化剂氧化,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
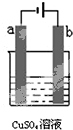 如图为直流电源电解1L 0.2mol/L的CuSO4水溶液的装置.通电一段时间后,b电极共收集到4.48L的气体(标准状况下),然后在石墨电极a和b附近分别滴加一滴石蕊试液,下列关于实验的叙述中不正确的是( )
如图为直流电源电解1L 0.2mol/L的CuSO4水溶液的装置.通电一段时间后,b电极共收集到4.48L的气体(标准状况下),然后在石墨电极a和b附近分别滴加一滴石蕊试液,下列关于实验的叙述中不正确的是( )| A、a电极的产物有Cu和H2 |
| B、反应一段时间后,溶液的pH值变小 |
| C、a电极附近呈红色,b电极附近出现蓝色 |
| D、a、b电极转移的电子数为0.8mol |
下列物质受光照射时,不会发生化学反应的是( )
| A、H2和Cl2混合 |
| B、H2和O2混合 |
| C、氯水 |
| D、AgBr |
下列应用不涉及氧化还原反应的是( )
| A、Na2O2用作呼吸面具的供氧剂 |
| B、工业上电解熔融状态Al2O3制备Al |
| C、工业上利用合成氨实现人工固氮 |
| D、实验室制二氧化碳 |
25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A、0.1mol?L-1 AlC13溶液中:H+、Na+、Cl-、SO42- |
| B、含有0.1mol?L-1 Fe3+的溶液中:Na+、K+、SCN-、NO3- |
| C、使甲基橙变红色的溶液中:Fe2+、K+、NO3-、SO42- |
| D、由水电离产生的c(H+)=10-12 mol?L-1的溶液中:NH4+、SO42-、HCO3-、Cl- |
X元素的阳离子和Y元素的阴离子具有与氩原子相同的电子层结构,下列叙述正确的是( )
| A、原子序数X>Y |
| B、最外层电子数X>Y |
| C、原子半径X<Y |
| D、最高正价X<Y |
下列叙述正确的是( )
| A、同周期元素中,VⅡA族元素的原子半径最大 |
| B、现已发现的零族元素的单质在常温常压下都是气体 |
| C、ⅥA族元素的原子,其半径越大,越容易得到电子 |
| D、所有的主族元素的简单离子的化合价与其族序数相等 |
下列指定反应的离子方程式正确的是( )
| A、向苯酚钠溶液中通入少量的CO2:C6H5O-+CO2+H2O→C6H5OH+HCO3- | ||||
| B、AlCl3溶液中加入少量氨水:Al3++3OH-=Al(OH)3↓ | ||||
| C、(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2↓ | ||||
D、用惰性电极电解氯化钠溶液:2Cl-+2H+
|