题目内容
氢离子浓度为1×10-3mol?Lˉ1的醋酸溶液20mL,用0.1mol?Lˉ1的氢氧化钠溶液10mL恰好完全中和,则醋酸的电离度是( )
| A、1% | B、2% | C、3% | D、4% |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:CH3COOH+NaOH=CH3COOH+H2O,根据方程式知CH3COOH、NaOH恰好完全中和,说明二者的物质的量相等,根据醋酸体积计算其浓度,再结合电离度公式计算醋酸电离度.
解答:
解:CH3COOH+NaOH=CH3COOH+H2O,根据方程式知CH3COOH、NaOH恰好完全中和,说明二者的物质的量相等,所以n(CH3COOH)=n(NaOH),设CH3COOH浓度为xmol/L,xmol/L×0.02L=0.1mol/L×0.01L,x=0.05,醋酸电离方程式为CH3COOH?H++CH3COO-,溶液中水、醋酸电离程度较小,所以水的电离忽略不计、溶液中电离部分醋酸浓度忽略不计,所以溶液中氢离子浓度等于电离醋酸浓度,所以电离度=
×100%=2%,
故选B.
| 10-3mol/L |
| 0.05mol/L |
故选B.
点评:本题考查了弱电解质的电离,正确理解电离度概念即可解答,注意计算其电离度时溶液中醋酸浓度、氢离子浓度的处理方法,题目难度不大.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
下列各种实验中不能达到实验目的是( )
A、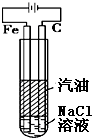 制备Fe(OH)2白色沉淀 |
B、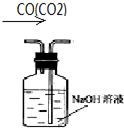 除去CO气体中的CO2气体 |
C、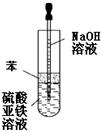 制备Fe(OH)2白色沉淀 |
D、 分离互不相溶的两种液体 |
下列有关物质的分类或归类不正确的是( )
①混合物:石炭酸、福尔马林、水玻璃、水银
②化合物:CaCl2、烧碱、苯乙烯、HD
③电解质:明矾、胆矾、冰醋酸、硫酸钡
④纯净物:干冰、冰水混合物、浓硫酸、水晶
⑤同位素:
C、
C、
C
⑥同系物:CH2O2、C2H4O2、C3H6O2、C4H8O2.
①混合物:石炭酸、福尔马林、水玻璃、水银
②化合物:CaCl2、烧碱、苯乙烯、HD
③电解质:明矾、胆矾、冰醋酸、硫酸钡
④纯净物:干冰、冰水混合物、浓硫酸、水晶
⑤同位素:
12 6 |
13 6 |
14 6 |
⑥同系物:CH2O2、C2H4O2、C3H6O2、C4H8O2.
| A、①②④⑥ | B、①②④⑤ |
| C、①③④⑤ | D、②④⑤⑥ |
反应:2SO2(g)+O2(g)?2SO3(g)(每生成2molSO3放出QKJ热量).在相同温度条件下,向一密闭恒容容器中通入2molSO2和1molO2达平衡时放出的热量为Q1,向另一容积相同的恒容密闭容器中通入1molSO2和0.5molO2达平衡时,放出的热量为Q2,则Q1、Q2满足的关系是( )
A、Q2=
| ||
B、Q2<
| ||
| C、Q2<Q1=Q | ||
| D、Q1=Q2<Q |
下列哪种情况没有发生Fe3+→Fe2+的转化( )
| A、过量的铁屑与稀硝酸混合 |
| B、将铁屑投入到稀盐酸溶液中 |
| C、用氯化铁溶液制作铜的印刷电路板 |
| D、把铁屑放入氯化铁溶液中 |
某溶液中含有的溶质是FeBr2、FeI2,若先向该溶液中通入一定量的氯气,再向反应后的溶液中滴加KSCN溶液,结果溶液变为红色(已知:AgBr、AgI分别为浅黄色和黄色不溶于硝酸的沉淀),则下列叙述正确的是( )
| A、原溶液中的Br-可能未被氧化 |
| B、反应后的溶液中是否含有Fe2+可以用氯水和KSCN溶液检验 |
| C、取所得溶液加入CCl4后静置分液,向上层溶液中加入足量AgNO3 溶液,能产生黄色沉淀 |
| D、反应后的溶液中一定不存在Fe2+ |
能说明醋酸是弱电解质的依据是( )
| A、醋酸能与碳酸钠反应,并有二氧化碳气体生成 |
| B、醋酸溶液能使紫色石蕊试液变红 |
| C、用醋酸溶液做导电性实验时,灯泡较暗 |
| D、在pH相等的醋酸和盐酸中,前者的物质的量浓度大得多 |