题目内容
(1)氨气(NH3)是一种无色有刺激性气味的气体,极易溶于水,其水溶液称为氨水,显碱性.实验室里通常用加热固体氯化铵和固体氢氧化钙的混合物的方法制取氨气,其化学方程式为:2NH4C1+Ca(OH)2=CaCl2+2NH3↑+2H2O.氨气在化工生产中应用广泛,如“侯氏制碱法”中就用到氨气.试回答下列问题:
①实验室制氨气的发生装置与 相同(选择“A或B”填空).
A.实验室用KMnO4制O2 B.实验室用大理石与稀盐酸制CO2
②收集氨气 用排水法收集(填“能或不能”).
③“侯氏制碱法”中关键一步的反应原理可表示为:NH3+CO2+H2O+NaCl=NaHCO3+X.
X是一种氮肥,其化学式为 .
(2)某同学为制备纯净干燥的氢气,准备了下图所示的A、B、C三种装置.其中A装置最大的特点是可以随时使反应发生或停止.

①装置A中发生反应的化学方程式为 .
②关闭弹簧夹时,A内的反应随即停止是因为 .
③为制备纯净干燥的氢气,A、B、C三种装置的连接顺序为 (填字母序号).
①实验室制氨气的发生装置与
A.实验室用KMnO4制O2 B.实验室用大理石与稀盐酸制CO2
②收集氨气
③“侯氏制碱法”中关键一步的反应原理可表示为:NH3+CO2+H2O+NaCl=NaHCO3+X.
X是一种氮肥,其化学式为
(2)某同学为制备纯净干燥的氢气,准备了下图所示的A、B、C三种装置.其中A装置最大的特点是可以随时使反应发生或停止.

①装置A中发生反应的化学方程式为
②关闭弹簧夹时,A内的反应随即停止是因为
③为制备纯净干燥的氢气,A、B、C三种装置的连接顺序为
考点:氨的实验室制法,常见气体制备原理及装置选择
专题:实验题
分析:(1)①根据实验室制取氨气选择固固加热装置,结合制取氧气、二氧化碳气体的反应原理来分析试剂和使用的仪器,从而确定装置;
②氨气极易溶于水;
③依据侯氏制碱法反应原理:氨气、二氧化碳通入饱和氯化钠反应生成碳酸氢钠和氯化铵解答;
(2)①锌与盐酸反应生成氢气;
②依据关闭弹簧夹时,反应产生的氢气使试管A内压强增大,盐酸被压入长颈漏斗与锌粒脱离接触解答;
③氢氧化钠溶液是除氯化氢杂质的,浓硫酸做干燥剂是除水蒸汽的,要注意最后才能除水蒸气.
②氨气极易溶于水;
③依据侯氏制碱法反应原理:氨气、二氧化碳通入饱和氯化钠反应生成碳酸氢钠和氯化铵解答;
(2)①锌与盐酸反应生成氢气;
②依据关闭弹簧夹时,反应产生的氢气使试管A内压强增大,盐酸被压入长颈漏斗与锌粒脱离接触解答;
③氢氧化钠溶液是除氯化氢杂质的,浓硫酸做干燥剂是除水蒸汽的,要注意最后才能除水蒸气.
解答:
解:(1)①实验室制备氨气和实验室用KMnO4制O2,都是固体与固体在加热条件下发生,实验室制备二氧化碳是固体与液体不加热,
故选:A;
②氨气极易溶于水,所以只能用排气法收集氨气,不能用排水法收集氨气;
故答案为:不能;
③依据“侯氏制碱法”反应原理结合原子个数守恒,可知NH3+CO2+H2O+NaCl=NaHCO3+NH4Cl,
故答案为:NH4Cl;
(2)①锌与盐酸反应生成氢气,反应的化学方程式为:Zn+2HCl=ZnCl2+H2↑,故答案为:Zn+2HCl=ZnCl2+H2↑;
②当关闭弹簧夹时,反应产生的氢气使试管A内压强增大,盐酸被压入长颈漏斗与锌粒脱离接触,反应停止,
故答案为:反应产生的氢气使试管A内压强增大,盐酸被压入长颈漏斗与锌粒脱离接触,反应停止;
③氢氧化钠溶液是除氯化氢杂质的,浓硫酸做干燥剂是除水蒸汽的,要注意最后才能除水蒸气,要制取纯净干燥的氯气A、B、C三种装置的连接顺序为A→B→C,
故答案为:A→B→C.
故选:A;
②氨气极易溶于水,所以只能用排气法收集氨气,不能用排水法收集氨气;
故答案为:不能;
③依据“侯氏制碱法”反应原理结合原子个数守恒,可知NH3+CO2+H2O+NaCl=NaHCO3+NH4Cl,
故答案为:NH4Cl;
(2)①锌与盐酸反应生成氢气,反应的化学方程式为:Zn+2HCl=ZnCl2+H2↑,故答案为:Zn+2HCl=ZnCl2+H2↑;
②当关闭弹簧夹时,反应产生的氢气使试管A内压强增大,盐酸被压入长颈漏斗与锌粒脱离接触,反应停止,
故答案为:反应产生的氢气使试管A内压强增大,盐酸被压入长颈漏斗与锌粒脱离接触,反应停止;
③氢氧化钠溶液是除氯化氢杂质的,浓硫酸做干燥剂是除水蒸汽的,要注意最后才能除水蒸气,要制取纯净干燥的氯气A、B、C三种装置的连接顺序为A→B→C,
故答案为:A→B→C.
点评:本题为是实验题,考查了氨气、氯气的实验室制备,题目难度不大,明确发生装置的选择是依据反应物的状态和反应的条件是解题关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
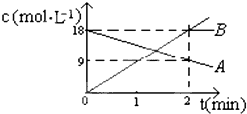 反应:A═2B中,A、B的浓度变化如图所示.则2min以内的平均反应的速率为( )
反应:A═2B中,A、B的浓度变化如图所示.则2min以内的平均反应的速率为( )| A、vA=9 mol/(L?min) |
| B、vA=4.5 mol?L?min |
| C、vB=18 mol/(L?min) |
| D、vB=9mol/(L?min) |
下列说法中,不正确的是( )
| A、光导纤维的主要成分是SiO2 |
| B、大量排放SO2会引起酸雨 |
| C、明矾和漂白粉均可用于自来水的杀菌、消毒 |
| D、玻璃和陶瓷都属于传统硅酸盐材料 |
下列说法正确的是( )
| A、SiO2是酸性氧化物,它可以与强碱反应,不能与任何酸反应 | ||||
B、根据SiO2+Na2CO3
| ||||
| C、CO2气体通入到Na2SiO3溶液中可以制得硅酸 | ||||
| D、SiO2可以与水反应生成相对应的酸--硅酸 |
糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同.下列分析正确的是( )
| A、脱氧过程是吸热反应,可降低温度,延长糕点保质期 |
| B、脱氧过程中铁作原电池正极,电极反应为:Fe-3e-=Fe3+ |
| C、脱氧过程中碳做原电池负极,电极反应为:2H2O+O2+4e-=4OH- |
| D、含有2.24g铁粉的脱氧剂,理论上最多能吸收氧气448mL(标准状况) |



