题目内容
19.碳酸锂是重要的锂化合物,是制备其它高纯锂化合物的重要原料.我国锂资源储量非常丰富,其中卤水锂资源约占其中的79%,由盐湖卤水(主要含有:LiCl、MgCl2、Na2B4O7等) 制备碳酸锂,其工艺流程如下: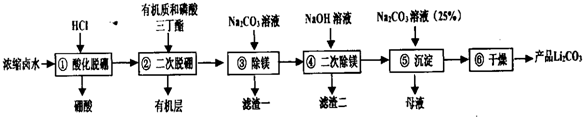
己知:
I、盐卤中的硼元素以Na2B4O7形式存在,硼酸(H3BO3)常温时在水中溶解度不大
Ⅱ、LiOH易溶于水
Ⅲ、
| 物质 | MgCO3 | Li2CO3 | Mg(OH)2 |
| Ksp | 6.82×10-6 | 8.2×10-4 | 5.6×10-12 |
(2)②过程中的操作名称是萃取反应,在所得有机层中加入0.25mol/LNaOH溶液可以再生有机质和磷酸三丁酯,但不能加浓NaOH溶液,其原因是避免氢氧化钠溶液浓度过大使磷酸三丁酯水解.
(3)③过程结束后,溶液中C(Li+)=5mol/L,若此过程中不产生Li2CO3沉淀,则此时溶液中镁离子的物质的量浓度不小于0.21mol/L.
(4)滤渣一,滤渣二的主要成分分别是MgCO3、Mg(OH)2.
(5)如何检验第⑤步中Li+是否沉淀完全取少量上层清液于试管中,继续加入碳酸钠溶液若无沉淀出现,则沉淀完全.
(6)髙纯度的碳酸锂可以用于制备锂离子电池的正极材料.如LiCoO2可以采用下面方法制备:将Li2CO3与CoCO3按1:1的比例混合,再在空气中灼烧即可,试写出该反应的化学方程式2Li2CO3+4CoCO3+O2$\frac{\underline{\;\;△\;\;}}{\;}$4LiCoO2+6CO2.
一种钻酸锂电池的工作原理如下:LixC6+Li1-xCoO2=LiCoO2+C6,该电池在充电时负极上发生的电极反应为xLi++xe-+C6=LixC6.
分析 浓缩卤水加入盐酸使大部分的B元素转化为硼酸(H3BO3)沉淀,再利用有机物和和磷酸三丁酯进行二次脱硼,萃取含有的B元素,通过分液分离出有机层,水层中加入碳酸钠进行除镁,滤渣一为碳酸镁,过滤后加入氢氧化钠溶液进行二次除镁,滤渣二为氢氧化镁,过滤后的滤液中加入碳酸钠溶液得到Li2CO3沉淀,过滤分离,母液中含有氯化钠等.
(1)过程①是Na2B4O7与盐酸反应生成H3BO3沉淀;
(2)②是利用机物和和磷酸三丁酯萃取含有的B元素,再通过分液分离;磷酸三丁酯在浓氢氧化钠溶液中会发生酯的水解反应;
(3)根据Li2CO3的溶度积计算c(CO32-),再结合MgCO3的溶度积计算c(Mg2+);
(4)滤渣一为碳酸镁,滤渣二为氢氧化镁;
(5)向上层清液中继续加入碳酸钠溶液,若无沉淀出现,说明沉淀完全;
(6)将Li2CO3与CoCO3按1:1的比例混合,再在空气中灼烧可得LiCoO2,Co元素化合物升高,发生氧化反应,有氧气参加反应,反应还生成二氧化碳;
一种钻酸锂电池的工作原理如下:LixC6+Li1-xCoO2=LiCoO2+C6,该电池在充电时负极上发生还原反应,C6获得电子生成LixC6.
解答 解:浓缩卤水加入盐酸使大部分的B元素转化为硼酸(H3BO3)沉淀,再利用有机物和和磷酸三丁酯进行二次脱硼,萃取含有的B元素,通过分液分离出有机层,水层中加入碳酸钠进行除镁,滤渣一为碳酸镁,过滤后加入氢氧化钠溶液进行二次除镁,滤渣二为氢氧化镁,过滤后的滤液中加入碳酸钠溶液得到Li2CO3沉淀,过滤分离,母液中含有氯化钠等.
(1)过程①是Na2B4O7与盐酸反应生成H3BO3沉淀,离子方程式为:B4O72-+2H++5H2O=4H3BO3↓,
故答案为:B4O72-+2H++5H2O=4H3BO3↓;
(2)②是利用机物和和磷酸三丁酯萃取含有的B元素,再通过分液分离,②过程中的操作名称是:萃取反应,磷酸三丁酯在浓氢氧化钠溶液中会发生酯的水解反应,
故答案为:萃取分液;避免氢氧化钠溶液浓度过大使磷酸三丁酯水解;
(3)溶液中c(Li+)=5mol/L,则此时溶液中c(CO32-)=$\frac{Ksp(L{i}_{2}C{O}_{3})}{{c}^{2}(L{i}^{+})}$=$\frac{8.2×1{0}^{-4}}{{5}^{2}}$mol/L=3.28×10-5mol/L,结合MgCO3的溶度积,可知溶液c(Mg2+)=$\frac{6.82×1{0}^{-6}}{3.28×1{0}^{-5}}$mol/L=0.21mol/L,
故答案为:0.21mol/L;
(4)滤渣一,滤渣二的主要成分分别是 MgCO3、Mg(OH)2,
故答案为:MgCO3、Mg(OH)2;
(5)检验第⑤步中Li+是否沉淀完全方法:取少量上层清液于试管中,继续加入碳酸钠溶液若无沉淀出现,则沉淀完全,
故答案为:取少量上层清液于试管中,继续加入碳酸钠溶液若无沉淀出现,则沉淀完全;
(6)将Li2CO3与CoCO3按1:1的比例混合,再在空气中灼烧可得LiCoO2,Co元素化合物升高,发生氧化反应,有氧气参加反应,反应还生成二氧化碳,反应方程式为:2Li2CO3+4CoCO3+O2$\frac{\underline{\;\;△\;\;}}{\;}$4LiCoO2+6CO2,
一种钻酸锂电池的工作原理如下:LixC6+Li1-xCoO2=LiCoO2+C6,该电池在充电时负极上发生还原反应,C6获得电子生成LixC6,电极反应式为:xLi++xe-+C6=LixC6,
故答案为:2Li2CO3+4CoCO3+O2$\frac{\underline{\;\;△\;\;}}{\;}$4LiCoO2+6CO2;xLi++xe-+C6=LixC6.
点评 本题是物质制备工艺流程题目,涉及物质分离提纯实验操作、对操作与原理的分析评价、溶度积有关计算、陌生方程式书写、电化学原理与电极反应式书写等,是对学生综合能力的考查,关键是对工艺流程的理解.

| A. | 氯气溶于水:H2O+Cl2═2H++ClOˉ+Clˉ | |
| B. | 锌片插入稀H2SO4溶液中:Zn+2H+═Zn2++H2↑ | |
| C. | 氢氧化钡溶液与稀硫酸反应:H++SO42-+OH-+Ba2+═H2O+BaSO4↓ | |
| D. | 碳酸钙溶于稀盐酸:CO32-+2H+═H2O+CO2↑ |
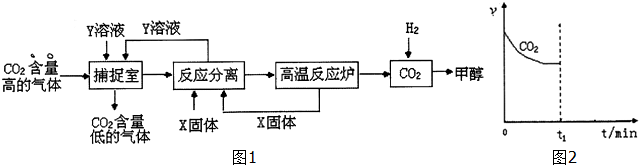
(1)下列有关捕捉空气中的CO2过程中的叙述不正确的有BD.
A、X选用CaO,而且要循环利用CaO与Y溶液
B、捕捉室里温度越高越有利于CO2 的捕捉
C、开放高效光催化剂分解水制氢气,是降低合成甲醇成本的有效途径
D、该捕捉CO2技术的应用有利于缓解全球变暖,而且能耗小
(2)在捕捉室用稀氨水喷淋“捕捉”空气中的CO2时,有NH2COONH4(氨基甲酸胺)生成.现将一定量纯净的氨基甲酸胺置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使反应
NH2COONH4(s)?2NH3(g)+CO2(g)达到分解平衡.实验测得不同温度及反应时间(t1<t2<t3)的有关表:氨基甲酸铵分解时温度、气体总浓度及反应时间的关系
 | 15 | 25 | 35 |
| 0 | 0 | 0 | 0 |
| t1 | 0.9×10-3 | 2.7×10-3 | 8.1×10-3 |
| t2 | 2.4×10-3 | 4.8×10-3 | 9.4×10-3 |
| t3 | 2.4×10-3 | 4.8×10-3 | 9.4×10-3 |
②根据表中数据换算出,15℃时合成反应2NH3(g)+CO2(g)?NH2COONH4(s)平衡常数K约为4.9×108.
(3)以捕捉到的CO2与H2为原料可合成甲醇(CH3OH),其反应的化学方程为:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g);△H<0.
①将1mol CO2和3mol H2充入恒温恒压的密闭容器中发生上述反应,CO2消耗速率v(CO2)与时间关系如图2所示.若在时间t1时,向容器中再充入1mol CO2和3mol H2,请在图中画出CH3OH生成速率v(CH3OH)与时间的关系曲线.
②在一个恒温固定容积的密闭容器中,加入1mol CO2和3mol H2,充分反应后达到平衡放出热量为aKJ.若在原来的容器中加入2mol CO2和6mol H2,在相同温度下充分反应,达到平衡放出热量为bKJ.则a和b满足的关系b>2a.
| A. | 室温下向1 L pH=1的醋酸溶液中加水,所得溶液的H+数目大于0.1NA | |
| B. | 60g乙酸与足量乙醇发生酯化反应,充分反应后断裂的C-O键数目为NA | |
| C. | 某无水乙醇与足量金属钠反应生成5.6 L H2,该乙醇分子中共价键总数为4 NA | |
| D. | 已知C2H4(g)+H2(g)═C2H6(g)△H=-137.0 kI/mol,乙烯与H2加成时放出68.5 kJ热量,则反应过程中被破坏的碳原子之间共用电子对数目为NA |
| A. | 合金的熔点一般比组分金属高 | B. | 合金中只含金属元素 | ||
| C. | 合金的机械性能一般比组分金属好 | D. | 合金的硬度一般比组分小 |
| A. | 钠在氧气中燃烧 | B. | NaOH溶液滴入NH4HCO3溶液 | ||
| C. | 稀硝酸中加入铁粉 | D. | 镁与H2SO4溶液 |
| A. | 碱 | B. | 氧化物 | C. | 酸 | D. | 盐 |
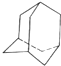 油田开采的石油中溶有一种碳氢化合物--金刚烷,它的分子立体结构如图所示:
油田开采的石油中溶有一种碳氢化合物--金刚烷,它的分子立体结构如图所示: