题目内容
在一定温度下,把2.0体积的N2和6.0体积的H2通入一个带活塞的体积可变的容器中,活塞的一端与大气相通,容器中发生如下反应:N2+3H2![]() 2NH3
2NH3
![]() 已知平衡时NH3的浓度是c mol·L-1,现按下列四种配比作为起始物质,分别充入上述容器,并保持温度不变,则达到平衡后,NH3的浓度不为c mol·L-1的是 ( )
已知平衡时NH3的浓度是c mol·L-1,现按下列四种配比作为起始物质,分别充入上述容器,并保持温度不变,则达到平衡后,NH3的浓度不为c mol·L-1的是 ( )
![]() A.1.0体积的N2和3.0体积的H2 B.2.0体积的N2、6.0体积的H2和4.0体积的NH3
A.1.0体积的N2和3.0体积的H2 B.2.0体积的N2、6.0体积的H2和4.0体积的NH3
![]() C.4.0体积的NH3和1.0体积的H2 D.2.0体积的NH3
C.4.0体积的NH3和1.0体积的H2 D.2.0体积的NH3
C
解析:
此题考查学生对恒温恒压条件下等效平衡的认识.恒温恒压建立等效平衡的条件是投料比相等.所以题设条件下,投入的N2和H2的体积比符合V(N2)∶V(H2)=2.0∶6.0=1∶3者皆可选.当然不论投入多少NH3,其转化为N2和H2的体积比皆为1∶3,即投入多少NH3都是合适的,或曰对等效平衡无影响.可见只有C选项可选.

练习册系列答案
相关题目
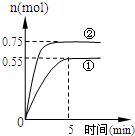 碳循环的途径之一是:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)+49.0kJ,在容积为2L的密闭容器中充入1mol CO2和3mol H2,在两种不同的实验条件下进行反应,测得CH3OH(g)的物质的量随时间变化情况如下图所示:
碳循环的途径之一是:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)+49.0kJ,在容积为2L的密闭容器中充入1mol CO2和3mol H2,在两种不同的实验条件下进行反应,测得CH3OH(g)的物质的量随时间变化情况如下图所示: