题目内容
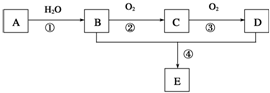 已知A是一种分子量为28的气态烃,现以A为主要原料合成一种具有果香味的物质E,其合成路线如图所示.
已知A是一种分子量为28的气态烃,现以A为主要原料合成一种具有果香味的物质E,其合成路线如图所示.请回答下列问题:
(1)写出A的结构简式
(2)B生成C的化学方程式
(3)物质B可以被直接氧化为D,需要加入的试剂是
(4)写出下列反应的化学方程式:
①
④
考点:有机物的推断
专题:有机物的化学性质及推断
分析:A 是一种分子量为28的气态烃,该烃是C2H4,乙烯和水发生加成反应生成B,B是乙醇CH3CH2OH,乙醇和氧气反应生成C,C是乙醛CH3CHO,乙醛和氧气反应生成D,D是乙酸 CH3COOH,乙醇和乙酸反应生成E,E是乙酸乙酯CH3COOCH2CH3,据此答题.
解答:
解:A 是一种分子量为28的气态烃,该烃是C2H4,乙烯和水发生加成反应生成B,B是乙醇CH3CH2OH,乙醇和氧气反应生成C,C是乙醛CH3CHO,乙醛和氧气反应生成D,D是乙酸 CH3COOH,乙醇和乙酸反应生成E,E是乙酸乙酯CH3COOCH2CH3.
(1)通过以上分析知,A是乙烯,其结构简式为CH2=CH2,故答案为CH2=CH2;
(2)B是乙醇,C是乙醛,B生成C的化学方程式为2CH3CH2OH+O2
2CH3CHO+2H2O,故答案为:2CH3CH2OH+O2
2CH3CHO+2H2O;
(3)乙醇可以被直接氧化为乙酸,需要加入的试剂是:酸性高锰酸钾溶液或酸性重铬酸钾溶液,
故答案为:酸性高锰酸钾溶液或酸性重铬酸钾溶液;
(4)在催化剂条件下,乙烯和水反应生成乙醇,反应方程式为CH2=CH2+H2
O CH3CH2OH,该反应是加成反应,乙酸和乙醇反应生成乙酸乙酯和水,乙酸中的羟基被-OCH2CH3取代生成乙酸乙酯,所以属于取代反应或置换反应,反应方程式为CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O;
故答案为:CH2=CH2+H2O
CH3CH2OH;加成反应;CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O;取代反应或酯化反应.
(1)通过以上分析知,A是乙烯,其结构简式为CH2=CH2,故答案为CH2=CH2;
(2)B是乙醇,C是乙醛,B生成C的化学方程式为2CH3CH2OH+O2
| 催化剂 |
| △ |
| 催化剂 |
| △ |
(3)乙醇可以被直接氧化为乙酸,需要加入的试剂是:酸性高锰酸钾溶液或酸性重铬酸钾溶液,
故答案为:酸性高锰酸钾溶液或酸性重铬酸钾溶液;
(4)在催化剂条件下,乙烯和水反应生成乙醇,反应方程式为CH2=CH2+H2
| 催化剂 |
| 浓H2SO4 |
| △ |
故答案为:CH2=CH2+H2O
| 催化剂 |
| 浓H2SO4 |
| △ |
点评:本题考查了有机物的推断,难度不大,明确物质具有的官能团确定其具有的性质,注意官能团的变化,答题时要注意基础知识的灵活运用.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
能说明氯化氢是共价化合物的事实是( )
| A、氯化氢不易分解 |
| B、液态氯化氢不导电 |
| C、氯化氢溶于水发生电离 |
| D、氯化氢水溶液显酸性 |
某酸的酸式盐NaHY在水溶液中,HY-的电离程度小于HY-的水解程度,有关叙述正确的是( )
| A、H2Y在电离时:H2Y+H2O?HY-+H3O+ |
| B、在该盐的溶液中,离子浓度为:c(Na+)>c(HY-)>c(Y2-)>c(OH-)>c(H+) |
| C、在该盐的溶液中,离子浓度为:c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+) |
| D、HY-水解方程式为:HY-+H2O?Y2-+H3O+ |
容量瓶上必须标明( )
①温度 ②浓度 ③容量 ④压强 ⑤刻度线.
①温度 ②浓度 ③容量 ④压强 ⑤刻度线.
| A、②③④ | B、①③⑤ | C、③④ | D、③ |
 乙酸是生活中的一种常见有机物,它的分子结构模型如图所示.
乙酸是生活中的一种常见有机物,它的分子结构模型如图所示.