题目内容
(1)有下列各组微粒或物质:
①CH4和C3H8 ②CH3CH(CH3)2和CH3CH2CH2CH3
③12C和14C ④ ⑤O2与O3
⑤O2与O3
以上各微粒或物质中互为同位素的是 ;互为同分异构体的是 ; 互为 同系物的是 ;属于同一种物质的是 .(用序号填写)
(2)0.1mol某烃完全燃烧,生成10.8g H2O和11.2LCO2(标准状况下).则该烃的分子式:
(3)下列有关实验操作、现象或结论的叙述正确的是
A.制备硝基苯的实验中,水浴加热可以较好的保持恒温条件.
B.乙醇的催化氧化实验中铜丝主要起氧化剂的作用.
C.制取乙酸乙酯时,试剂加入的顺序是:先加入乙醇,后慢慢加入浓硫酸,最后加入乙酸.
D.除去甲烷中混有的少量乙烯,可以将混合气体通过酸性KMnO4溶液
E.用钠可以检验某无水酒精中是否含有水.
①CH4和C3H8 ②CH3CH(CH3)2和CH3CH2CH2CH3
③12C和14C ④
 ⑤O2与O3
⑤O2与O3以上各微粒或物质中互为同位素的是
(2)0.1mol某烃完全燃烧,生成10.8g H2O和11.2LCO2(标准状况下).则该烃的分子式:
(3)下列有关实验操作、现象或结论的叙述正确的是
A.制备硝基苯的实验中,水浴加热可以较好的保持恒温条件.
B.乙醇的催化氧化实验中铜丝主要起氧化剂的作用.
C.制取乙酸乙酯时,试剂加入的顺序是:先加入乙醇,后慢慢加入浓硫酸,最后加入乙酸.
D.除去甲烷中混有的少量乙烯,可以将混合气体通过酸性KMnO4溶液
E.用钠可以检验某无水酒精中是否含有水.
考点:同位素及其应用,芳香烃、烃基和同系物,同分异构现象和同分异构体,有关有机物分子式确定的计算
专题:原子组成与结构专题,同系物和同分异构体,烃及其衍生物的燃烧规律
分析:(1)具有相同质子数,不同中子数(或不同质量数)同一元素的不同核素互为同位素;同系物是有机化合物中具有同一通式、组成上相差一个或多个CH2原子团、在结构与性质上相似的化合物系列;具有相同分子式而结构不同的化合物互为同分异构体;同种元素形成的不同单质互为同素异形体;
(2)计算二氧化碳、水的物质的量,根据原子守恒确定烃的分子式;
(3)A.水浴加热时温度容易控制;
B.乙醇的催化氧化实验中铜丝起到催化剂的作用;
C.浓硫酸稀释时放热,则应该把浓硫酸加入到其它液体中;
D.乙烯和酸性高锰酸钾反应生成二氧化碳气体;
E.钠可与乙醇、水都反应.
(2)计算二氧化碳、水的物质的量,根据原子守恒确定烃的分子式;
(3)A.水浴加热时温度容易控制;
B.乙醇的催化氧化实验中铜丝起到催化剂的作用;
C.浓硫酸稀释时放热,则应该把浓硫酸加入到其它液体中;
D.乙烯和酸性高锰酸钾反应生成二氧化碳气体;
E.钠可与乙醇、水都反应.
解答:
解:(1)①CH4和C3H8 都属于烷烃,是同系物;
②CH3CH(CH3)2和CH3CH2CH2CH3具有相同分子式而结构不同互为同分异构体;
③12C和14C 具有相同质子数,不同中子数(或不同质量数)同一元素的不同核素互为同位素;
④ 二者结构为正四面体,结构相同,分子式相同,属于同种物质;
二者结构为正四面体,结构相同,分子式相同,属于同种物质;
⑤O2与O3都是氧元素形成的单质,属于同素异形体;
故答案为:③;②;①;④;
(2)0.1mol某烃完全燃烧,生成10.8g H2O和11.2LCO2(标准状况下),则11.2LCO2的物质的量=
=0.5mol,10.8g H2O的物质的量=
=0.6mol,故该烃分子中C原子数目=
=5,H原子数目=
=12,故烃的分子式为C5H12,
故答案为:C5H12;
(3)A.制备硝基苯的实验中,水浴加热使反应物受热均匀,温度便于控制,可以较好的保持恒温条件,故A正确;
B.乙醇的催化氧化实验中,铜丝在反应前后质量和性质都不变化,起到催化剂的作用,故B错误;
C.浓硫酸稀释时放热,所以先加乙醇,再加浓硫酸,最后加入醋酸,故C正确;
D.乙烯和酸性高锰酸钾反应生成二氧化碳气体,引入新杂质,应用溴水除杂,故D错误;
E.钠可与乙醇、水都反应,应用硫酸铜检验,故E错误.
故答案为:AC.
②CH3CH(CH3)2和CH3CH2CH2CH3具有相同分子式而结构不同互为同分异构体;
③12C和14C 具有相同质子数,不同中子数(或不同质量数)同一元素的不同核素互为同位素;
④
 二者结构为正四面体,结构相同,分子式相同,属于同种物质;
二者结构为正四面体,结构相同,分子式相同,属于同种物质;⑤O2与O3都是氧元素形成的单质,属于同素异形体;
故答案为:③;②;①;④;
(2)0.1mol某烃完全燃烧,生成10.8g H2O和11.2LCO2(标准状况下),则11.2LCO2的物质的量=
| 11.2L |
| 22.4L/mol |
| 10.8g |
| 18g/mol |
| 0.5mol |
| 0.1mol |
| 0.6mol×2 |
| 0.1mol |
故答案为:C5H12;
(3)A.制备硝基苯的实验中,水浴加热使反应物受热均匀,温度便于控制,可以较好的保持恒温条件,故A正确;
B.乙醇的催化氧化实验中,铜丝在反应前后质量和性质都不变化,起到催化剂的作用,故B错误;
C.浓硫酸稀释时放热,所以先加乙醇,再加浓硫酸,最后加入醋酸,故C正确;
D.乙烯和酸性高锰酸钾反应生成二氧化碳气体,引入新杂质,应用溴水除杂,故D错误;
E.钠可与乙醇、水都反应,应用硫酸铜检验,故E错误.
故答案为:AC.
点评:本题考查较为综合,涉及同位素、同分异构体、同系物等概念的理解、物质的分离、检验、制备以及乙醇的催化氧化等知识,侧重于学生的分析能力、实验能力和评价能力的考查,注意把握实验的原理和操作的严密性,难度中等.

练习册系列答案
相关题目
已知在一定条件下2A(g)+B(g)?3C(g)△H=+Q kJ?mol-1.向一个容积不变的密闭容器甲中加入2mol A和1mol B,达平衡时A的转化率为90%,吸收的热量为Q1kJ;向另一个密闭容器乙中加入一定量C,达到平衡时C的浓度与甲相同,放出的热量为Q2 kJ,则下说法中正确的是( )
| A、起始时C的物质的量及C的转化率一定为3 mol和10% |
| B、Q1>Q2 |
| C、Q2一定小于Q1 |
| D、若乙容器是一个体积不变的绝热容器,则反应达平衡后,乙中的压强一定大于甲 |

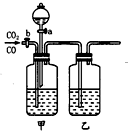 为将CO2和CO进行分离并得到干燥的CO2和CO,现设计一套装置(如图).
为将CO2和CO进行分离并得到干燥的CO2和CO,现设计一套装置(如图).