题目内容
下列关于化学键的说法正确的是( )
| A、由于金属键具有方向性与饱和性,所以金属在外加电场作用下导电 |
| B、金属键是金属阳离子与自由电子间的相互作用 |
| C、氢键、配位键都是特殊的共价键 |
| D、离子晶体中只存在离子键 |
考点:化学键
专题:
分析:A.金属导电与自由电子无关;
B.金属阳离子带正电,自由电子带负电;
C.氢键、配位键都以共用电子对成键;
D.离子晶体中可存在共价键.
B.金属阳离子带正电,自由电子带负电;
C.氢键、配位键都以共用电子对成键;
D.离子晶体中可存在共价键.
解答:
解:A.金属导电与自由电子无关,与方向性、饱和性无关,故A错误;
B.金属阳离子带正电,自由电子带负电,则金属键是金属阳离子与自由电子间的相互作用,故B正确;
C.氢键、配位键都以共用电子对成键,均属于共价键,故C正确;
D.离子晶体中一定存在离子键,可存在共价键,如NaOH等,故D错误;
故选BC.
B.金属阳离子带正电,自由电子带负电,则金属键是金属阳离子与自由电子间的相互作用,故B正确;
C.氢键、配位键都以共用电子对成键,均属于共价键,故C正确;
D.离子晶体中一定存在离子键,可存在共价键,如NaOH等,故D错误;
故选BC.
点评:本题考查化学键,为高频考点,把握化学键形成的一般规律及常见物质中的化学键为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
下列各种仪器:①漏斗、②容量瓶、③量筒、④分液漏斗、⑤天平、⑥胶头滴管、⑦蒸馏烧瓶,常用于物质分离的是( )
| A、①③⑦ | B、①④⑦ |
| C、②③⑥ | D、③④⑦ |
下列能用勒沙特列原理解释的是( )
| A、由二氧化硫和氧气反应制三氧化硫需要使用催化剂 |
| B、棕红色NO2加压后颜色先变深后变浅 |
| C、SO2催化氧化成SO3的反应,往往需要使用催化剂 |
| D、H2、I2、HI平衡混合气加压后颜色变深 |
已知X、Y分别为同周期的ⅠA和 VIA族的两种元素,它们的原子序数分别为a和b,则下列关系不可能成立的是( )
| A、a=b-15 |
| B、a=b-29 |
| C、a=b-9 |
| D、a=b-5 |
下列说法中正确的是( )
| A、22.4LO2中一定含有6.02×1023个氧分子 |
| B、将80gNaOH固体溶于1L水中,所得溶液中NaOH的物质的量浓度为2mol/L |
| C、18gH2O在标准状况下的体积是22.4L |
| D、在标准状况时,20mLNH3与60mLO2所含的分子数之比为1:3 |
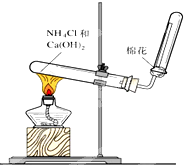 如图是实验室制取和收集氨气的装置图.回答下列问题:
如图是实验室制取和收集氨气的装置图.回答下列问题: