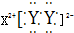题目内容
10.向一个2L容密闭容器中充入3.6molN2和10.8molH2,一定的条件下反应生成NH3,10min后测得N2的浓度是0.8mol•L-1,则在这10min内NH3的平均反应速率是( )| A. | 0.1 mol•L-1•min-1 | B. | 0.2 mol•L-1•min-1 | ||
| C. | 0.3 mol•L-1•min-1 | D. | 0.6 mol•L-1•min-1 |
分析 利用三段式可求得平衡时各成分的浓度,结合公式v(NH3)=$\frac{△c}{△t}$,进而求得反应速率.
解答 解:利用三段式
N2 +3H2 ?2NH3
起始量(mol/L) $\frac{3.6mol}{2L}$ $\frac{10.8mol}{2L}$ 0
变化量(mol/L) 1mol/L 3mol/L 2mol/L
2min量(mol/L) 0.8mol/L 2.4mol/L 2mol/L
则在这10min内NH3的平均反应速率是v(NH3)=$\frac{△c}{△t}$=$\frac{2mol/L}{10min}$=0.2mol/(L•min),
故选B.
点评 本题考查化学反应速率计算,把握化学反应速率计算公式及运用好三段式的计算方法是解答关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.下面是某科学兴趣小组的同学做同周期元素性质递变规律的实验时,设计了一套实验方案.其中实验步骤如下:
请整理并完成实验报告.
(1)实验目的:探究同周期元素性质的递变规律.
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na 2S溶液,AlCl 3溶液,NaOH溶液等.
仪器:①试管,②酒精灯,③胶头滴管,试管夹,镊子,小刀,玻璃片,砂纸等.
(3)实验内容:(完成下列表格中的实验现象和化学方程式)
(4)实验结论:同周期元素随原子序数的递增,失电子能力逐渐减弱,得电子能力逐渐增强.
(5)请用原子结构的知识简单解释上述结论.
| 实验序号 | 实验步骤 |
| ① | 将镁条用砂纸打磨后,放入沸水中;再向溶液中滴加酚酞溶液 |
| ② | 向新制得的Na 2S溶液中滴加新制的氯水 |
| ③ | 将一小块金属钠放入滴有酚酞溶液的冷水中 |
| ④ | 将镁条投入稀盐酸中 |
| ⑤ | 将铝条投入稀盐酸中 |
| ⑥ | 向AlCl 3溶液中滴加NaOH溶液至过量 |
(1)实验目的:探究同周期元素性质的递变规律.
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na 2S溶液,AlCl 3溶液,NaOH溶液等.
仪器:①试管,②酒精灯,③胶头滴管,试管夹,镊子,小刀,玻璃片,砂纸等.
(3)实验内容:(完成下列表格中的实验现象和化学方程式)
| 实验序号 | 实验步骤(略) | 实验现象 | 化学方程式 |
| ① | |||
| ② | |||
| ③ | |||
| ④ | |||
| ⑤ | |||
| ⑥ |
(5)请用原子结构的知识简单解释上述结论.
5.下列关系正确的是( )
| A. | 熔点:正戊烷>2,2一二甲基戊烷>2,3一二甲基丁烷>丙烷 | |
| B. | 密度:CCl4>H2O>苯 | |
| C. | 同质量的物质燃烧耗O2量:丙炔>乙烷>乙烯>乙炔>甲烷 | |
| D. | 同物质的量物质燃烧耗O2量:已烷>环已烷>苯>苯甲酸 |
15.欲制取较纯净的CH2ClCH2Cl,可采取的方法是( )
| A. | 乙烷与Cl2取代 | B. | 乙烯与Cl2加成 | ||
| C. | 乙炔与HCl加成 | D. | 乙醇与浓盐酸取代 |
19.乙烯可通过石油裂解获得.下列有关乙烯性质的说法错误的是( )
| A. | 在常温常压下为液体 | B. | 能使酸性KMnO4溶液褪色 | ||
| C. | 可自身加成形成聚乙烯 | D. | 能使溴的CCl4溶液褪色 |
20.下表是周期表中的一部分,根据A~M在周期表中的位置,回答下列问题:
(1)表中元素,化学性质最不活泼的是Ne,氧化性最强的单质是F2,还原性最强的单质是Na.(写元素符号或化学式)
(2)表中元素的最高价氧化物对应的水化物中,碱性最强的化合物的化学式为NaOH,酸性最强的化合物的化学式为HClO4,呈两性的化合物的化学式为Al(OH)3.
(3)A分别与B、C、D、E、J、K、L、M形成的化合物中最稳定的是HF(写化学式).
(4)写出D、G、L对应的离子半径由大到小的顺序:S2->O2->Na+(用离子符号表示).
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | B | C | D | E | F | |||
| 3 | G | H | I | J | K | L | M |
(2)表中元素的最高价氧化物对应的水化物中,碱性最强的化合物的化学式为NaOH,酸性最强的化合物的化学式为HClO4,呈两性的化合物的化学式为Al(OH)3.
(3)A分别与B、C、D、E、J、K、L、M形成的化合物中最稳定的是HF(写化学式).
(4)写出D、G、L对应的离子半径由大到小的顺序:S2->O2->Na+(用离子符号表示).
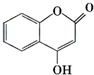 可用来制备抗凝血药,通过下列路线合成:
可用来制备抗凝血药,通过下列路线合成: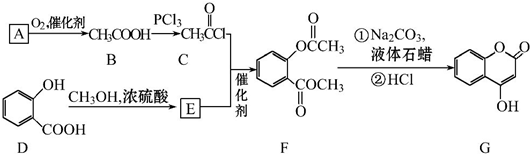
 .
. +3NaOH$\stackrel{△}{→}$
+3NaOH$\stackrel{△}{→}$ +CH3COONa+CH3OH+H2O.
+CH3COONa+CH3OH+H2O.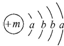 ,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.