题目内容
将4mol SO2与2molO2放入4L的密闭容器中,在一定条件下反应达到平衡: 2SO2+O2
2SO2+O2 2SO3,测得平衡时SO3的浓度为0.5mol/L,求:
2SO3,测得平衡时SO3的浓度为0.5mol/L,求:
 (1)平衡时各反应物的浓度;
(1)平衡时各反应物的浓度;
 (2)平衡时SO2的转化率;
(2)平衡时SO2的转化率;
 (3)该条件下的平衡常数K
(3)该条件下的平衡常数K
(1)c(SO2)=0.5 mol/L  ;c(O2)=0.25 mol/L c(SO3)=0.5mol/L ;(2)50%;(3)4
;c(O2)=0.25 mol/L c(SO3)=0.5mol/L ;(2)50%;(3)4
【解析】
试题分析:设有已转化的SO2为X mol
 2SO2+O2
2SO2+O2 2SO3
2SO3
 起始(mol) 4 2 0
起始(mol) 4 2 0
 转化(mol) X 0.5X X
转化(mol) X 0.5X X
 平衡(mol) 4-X 2-0.5X X
平衡(mol) 4-X 2-0.5X X
 解得X=4×0.5=2 mol
解得X=4×0.5=2 mol  (1)平衡时各物质的浓度为:C(SO2)=(4-2) mol/4L=0.5 mol/L
(1)平衡时各物质的浓度为:C(SO2)=(4-2) mol/4L=0.5 mol/L  ;C(O2)=(2-1) mol/4L=0.25 mol/L
;C(O2)=(2-1) mol/4L=0.25 mol/L  ;(2)平衡时SO2的转化率为: (2/4) ×100% = 50%
;(2)平衡时SO2的转化率为: (2/4) ×100% = 50%  ;(3)K=4
;(3)K=4
考点:化学平衡常数

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 成金属氢化物的材料
成金属氢化物的材料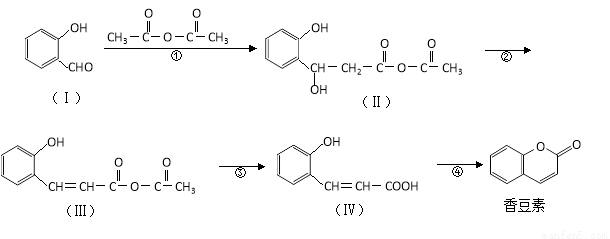
 与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物
与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物