题目内容
7.用NA表示阿伏德罗常数,下列叙述正确的是( )| A. | 标准状况下,22.4LH2O含有的分子数为 NA | |
| B. | 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA | |
| C. | 物质的量浓度为1mol/L的MgCl2溶液中,含有Cl-个数为2NA | |
| D. | 通常状况下,NA 个CO2分子占有的体积为22.4L |
分析 A、标准状况下,水的状态不是气体,不能使用标况下的气体摩尔体积计算水的物质的量;
B、1.06g碳酸钠的物质的量为0.01mol,0.01mol碳酸钠中含有0.02mol钠离子;
C、没有告诉氯化镁溶液的体积,无法计算溶液中氯离子的物质的量;
D、不是标准状况下,不能使用标况下的气体摩尔体积计算二氧化碳的体积.
解答 解:A.标况下水的状态不是气体,不能使用标况下的气体摩尔体积计算22.4L水的物质的量,故A错误;
B、1.06g碳酸钠的物质的量为0.01mol,含有0.02mol钠离子,含有的Na+离子数为0.02 NA,故B正确;
C、题中没有告诉1mol/L的MgCl2溶液的体积,无法计算氯离子的数目,故C错误;
D、通常状况下,不能使用标况下的气体摩尔体积计算二氧化碳的体积,故D错误;
故选B.
点评 本题考查阿伏加德罗常数的应用,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下气体摩尔体积的使用条件,试题有利于提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
18.最近《科学》杂志评出10大科技突破,其中“火星上‘找’到水的影子”名列第一.下列关于水的说法中正确的是( )
| A. | 水的离子积仅适用于纯水 | |
| B. | 水的电离需要直流电 | |
| C. | 升高温度水的离子积增大 | |
| D. | 加入电解质一定会破坏水的电离平衡 |
15.将AlCl3溶液和NaAlO2溶液分别蒸干灼烧,对产物的主要成分叙述正确的是( )
| A. | 均为Al(OH)3 | B. | 前者为Al2O3,后者为NaAlO2 | ||
| C. | 均为Al2O3 | D. | 前者为AlCl3,后者为NaAlO2 |
2.类推法是化学学习和研究中常用的重要思维方法,但所得结论要经过实践的检验才能确定其正确与否.根据你所掌握的知识,判断下列类推结论中正确的是( )
| 化学事实 | 类推结论 | |
| A | 卤素单质的沸点:F2<Cl2<Br2<I2 | 氢化物沸点:HF<HCl<HBr<HI |
| B | 用电解熔融MgCl2可制得金属镁 | 用电解熔融NaCl也可以制取金属钠 |
| C | 将CO2通入Ba(NO3)2溶液中无沉淀生成 | 将SO2通入Ba(NO3)2溶液中也无沉淀生成 |
| D | Al与S加热时直接化合生成Al2S3 | Fe与S加热时也能直接化合生成 Fe2S3 |
| A. | A | B. | B | C. | C | D. | D |
12.100mL 6mol/L的硫酸跟过量锌粉反应,在一定温度下,为了减缓反应速率,但又不影响生成氢气的总量,可向反应物中加入适量的( ) ①硫酸钠固体,②醋酸钠固体,③硫酸钾溶液,④硝酸钾溶液.
| A. | ①② | B. | ③④ | C. | ②③ | D. | ②③④ |
19.下列说法正确的是( )
| A. | 共价化合物中一定不含离子键 | |
| B. | 离子化合物中一定不含共价键 | |
| C. | 金属越活泼金属键越强 | |
| D. | 双原子分子中共价键越强,沸点越高 |
16. 如表为元素周期表的一部分.
如表为元素周期表的一部分.
回答下列问题:
(1)Z元素在周期表中的位置为第三周期、第ⅦA族.
(2)表中元素原子半径最大的是(填元素符号)Si.
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是ac.
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)沸点:H2Y>H2S(填“>”或“=”或“<”),理由是H2O分子间有氢键,氢键比分子间作用力强.
(5)Y2和Y3互为同素异形体(填“同位素”或“同分异构体”或“同素异形体”).
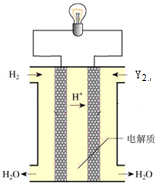
(6)其中单质Y2可用做如图所示装置(燃料电池)的氧化剂,请写出Y2在酸性电解质溶液中发生的电极反应方程式O2+4e-+4H+=2H2O.
 如表为元素周期表的一部分.
如表为元素周期表的一部分.| 碳 | 氮 | Y | |
| X | 硫 | Z |
(1)Z元素在周期表中的位置为第三周期、第ⅦA族.
(2)表中元素原子半径最大的是(填元素符号)Si.
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是ac.
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)沸点:H2Y>H2S(填“>”或“=”或“<”),理由是H2O分子间有氢键,氢键比分子间作用力强.
(5)Y2和Y3互为同素异形体(填“同位素”或“同分异构体”或“同素异形体”).
(6)其中单质Y2可用做如图所示装置(燃料电池)的氧化剂,请写出Y2在酸性电解质溶液中发生的电极反应方程式O2+4e-+4H+=2H2O.