题目内容
7.完成下列各小题:(1)在CuSO4溶液中滴入少量稀氨水,现象是:出现淡蓝色沉淀,反应的离子方程式为Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+;继续滴入过量稀氨水,发现难溶物溶解并生成深蓝色溶液,测得该溶液中的主要离子是[Cu(NH3)4 (H2O)2]2+,已知该配离子空间构型呈八面体形,则铜离子的杂化方式为sp3d2,配体有2种,配体分子的空间构型依次是三角锥形;V形.
(2)写出27Co3+离子的价电子排布式3d6,已知钴27Co3+的配位数为6,有一种组成为Co(NH3)5Cl3的配合物,取此配合物1mol与足量AgNO3溶液反应仅能析出2molAgCl沉淀,则该配合物的化学式为:[Co(NH3)5Cl]Cl2.
分析 (1)在CuSO4溶液中滴入少量稀氨水会生成氢氧化铜沉淀;氢氧化铜能溶于过量的氨水;[Cu(NH3)4 (H2O)2]2+中NH3中N原子和H2O中O原子提供孤对电子,Cu2+提供空轨道;NH3分子中孤对电子数为1,成键数为3,H2O中O原子中孤对电子数为2,成键数为2;
(2)Co的原子序数为27,价电子排布为3d74s2;配合物中配位离子Cl-不与Ag+反应,1mol该配合物生成2mol AgCl沉淀,据此计算出外界离子Cl-离子的数目判断,据此分析解答.
解答 解:(1)在CuSO4溶液中滴入少量稀氨水会生成氢氧化铜沉淀,即出现淡蓝色沉淀,其反应的离子方程式为Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+;氢氧化铜能溶于过量的氨水;已知[Cu(NH3)4 (H2O)2]2+空间构型呈八面体形,则铜离子的杂化方式为sp3d2,[Cu(NH3)4 (H2O)2]2+中NH3中N原子和H2O中O原子提供孤对电子,Cu2+提供空轨道,所以配体有2种;NH3分子中孤对电子数为1,成键数为3,氨气的空间构型为三角锥形,H2O中O原子中孤对电子数为2,成键数为2,所以H2O分子的空间构型为V形;
故答案为:出现淡蓝色沉淀;Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+;sp3d2;2;三角锥形;V形;
(2)Co的原子序数为27,价电子排布为3d74s2,则基态27Co3+离子的价电子排布式3d6;配合物中配位离子Cl-不与Ag+反应,1mol该配合物生成2mol AgCl沉淀,所以1mol该配合物中含2mol外界离子Cl-,即配离子中含有2个Cl-,又由于Co3+配位数为6,则NH3配位数为5,故该配合物的化学式可写为:[Co(NH3)5Cl]Cl2,
故答案为:3d6;[Co(NH3)5Cl]Cl2.
点评 本题考查较综合,涉及电子排布、离子方程式的书写、杂化方式、分子空间构型的判断、配合物等,侧重原子结构与性质的考查,题目难度中等,侧重于考查学生对基础知识的应用能力.

| A. | (CH3)3 C-CH=CH2 | B. | CH3CH=C(CH3)C (CH3)3 | ||
| C. | HC≡CCH(CH3)C(CH3)3 | D. | (CH3)3CC(CH3)=CHCH3 |
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、C(石墨) | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | 氢氧化钠溶液 | 偏向Mg |
| 5 | Al、Zn | 浓硝酸 | 偏向Al |
(2)对实验3完成下列填空:铝为负极,电极反应2Al-6e-═2Al3+;石墨为正极,电极反应6H++6e-═3H2↑;
(3)实验4中铝作负极还是正极负极,铝电极的电极反应Al-3e-+4OH-═AlO2-+2H2O.
| A. | 五氯化磷 | B. | 光气(化学式为:COCl2) | ||
| C. | 二硫化碳 | D. | 三氯化硼 |
| A. | 一定条件下,苯与浓硫酸和浓硝酸的混合液生成硝基苯 | |
| B. | 乙烯在催化剂作用下水化成乙醇 | |
| C. | 钠在乙醇中生成乙醇钠 | |
| D. | 水壶中的水垢通常用醋洗去 |

| A. | N2 | B. | H2S | C. | Mg | D. | Na |
| A. | 粘有油脂的试管可以用热的纯碱溶液洗涤 | |
| B. | 食醋中含有乙酸,乙酸可由乙醇氧化得到 | |
| C. | 煤的气化、液化只发生物理变化 | |
| D. | 天然气作为化工原料主要用于合成氨和合成甲醇 |
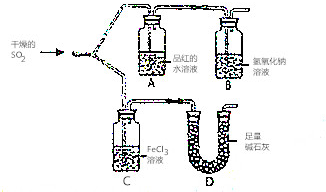 如图装置进行SO2气体性质实验
如图装置进行SO2气体性质实验