题目内容
雾霾天气严重影响人们的生活质量,其中氮氧化物和硫氧化物是造成雾霾天气的主要原因之一.
Ⅰ.将PM2.5样本用蒸馏水处理制成待测试样.
若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断该试样的pH= .
Ⅱ.消除氮氧化物和硫氧化物有多种方法.
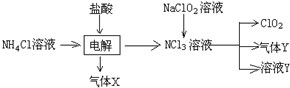
(1)方法一:工业上变“废”为宝,吸收工业中SO2和NO,可获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):

①装置Ⅰ中的主要反应的离子方程式为 .
②装置Ⅲ还可以使Ce4+再生,若用甲烷燃料电池电解该装置中的溶液,当消耗1mol甲烷时,理论上可再生 molCe4+.
(2)方法二:NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术.反应原理如图1所示: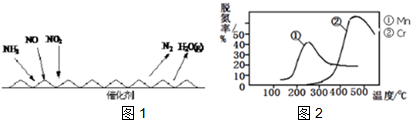
①图2是不同催化剂Mn和Cr在不同温度下对应的脱氢率,由图综合考虑可知最佳的催化剂和相应的温度分别为: (填序号).
a.Mn,200℃左右 b.Cr,450℃左右 c.Mn和Cr混合,300℃左右
②用Fe做催化剂时,在氨气足量的情况下,若
=1:1对应的脱氢率最佳,已知每生成11.2LN2(标)反应放出的热量为QkJ,此时对应的脱氢反应的热化学方程式为 .
Ⅰ.将PM2.5样本用蒸馏水处理制成待测试样.
若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol?L-1 | 3×10-6 | 7×10-6 | 3×10-5 | 3×10-5 | 5×10-5 | 2×10-5 |
Ⅱ.消除氮氧化物和硫氧化物有多种方法.
(1)方法一:工业上变“废”为宝,吸收工业中SO2和NO,可获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):

①装置Ⅰ中的主要反应的离子方程式为
②装置Ⅲ还可以使Ce4+再生,若用甲烷燃料电池电解该装置中的溶液,当消耗1mol甲烷时,理论上可再生
(2)方法二:NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术.反应原理如图1所示:

①图2是不同催化剂Mn和Cr在不同温度下对应的脱氢率,由图综合考虑可知最佳的催化剂和相应的温度分别为:
a.Mn,200℃左右 b.Cr,450℃左右 c.Mn和Cr混合,300℃左右
②用Fe做催化剂时,在氨气足量的情况下,若
| c(NO2) |
| c(NO) |
考点:物质分离和提纯的方法和基本操作综合应用,化学平衡的调控作用,pH的简单计算
专题:
分析:Ⅰ、依据电荷守恒,计算溶液中含有的是氢离子还是氢氧根,然后计算pH值即可;
Ⅱ、(1)①二氧化硫是酸性氧化物,能和强碱之间发生反应;
②1molCe3+再生转化为Ce4+,提供电子为1mol,1mol甲烷完全燃烧,转移电子为mol,据此解答即可;
(2)①温度越高,对设备的要求越高,所以如果催化剂在较低温度下能较大程度的脱氢即可;根据纵坐标判断,相同温度下,脱氢率越高的效果越好;生成1mol氮气放出QkJ热量,则生成2mol氮气放出2QkJ热量.
Ⅱ、(1)①二氧化硫是酸性氧化物,能和强碱之间发生反应;
②1molCe3+再生转化为Ce4+,提供电子为1mol,1mol甲烷完全燃烧,转移电子为mol,据此解答即可;
(2)①温度越高,对设备的要求越高,所以如果催化剂在较低温度下能较大程度的脱氢即可;根据纵坐标判断,相同温度下,脱氢率越高的效果越好;生成1mol氮气放出QkJ热量,则生成2mol氮气放出2QkJ热量.
解答:
解:Ⅰ、溶液中遵循电荷守恒:c(K+)+c(NH4+)+c(Na+)+c(H+)=2c(SO42-)+c(NO3-)+c(Cl-)+c(OH-)和KW,即:3×10-6+7×10-6+3×10-5+c(H+)=2×3×10-5+5×10-5+2×10-5,解c(H+)=10-4mol?L-1,pH值为4,故答案为:4;
Ⅱ、(1)①二氧化硫是酸性氧化物,能和强碱氢氧化钠之间发生反应:SO2+OH-=HSO3-,NO和氢氧化钠之间不会反应,故答案为:SO2+OH-=HSO3-;
②甲烷燃料电池中,在碱性溶液中,甲烷燃料电池的负极反应式为CH4-8e-+10OH-═CO32-+7H2O,故每有1mol甲烷反应,转移电子数为8mol,每生成1molCe4+,提供电子为1mol,故答案为:8;
(2)①根据图象知,脱氢率越高越好,但Cr作催化剂时温度高于Mn,温度越高,对设备要求越高,增大生产成本,且脱氢率增大较小,所以使用Mn作催化剂较好;根据图象知,在温度为200-250℃或范围内间任意温度,脱氢率较高,故答案为:a;
②生成0.5mol氮气放出QkJ热量,则生成2mol氮气放出4QkJ热量,则其热化学反应方程式为2NH3(g)+NO(g)+NO2(g)?2N2(g)+3H2O(g)△H=-4QkJ/mol,
故答案为:2NH3(g)+NO(g)+NO2(g)?2N2(g)+3H2O(g)△H=-4QkJ/mol.
Ⅱ、(1)①二氧化硫是酸性氧化物,能和强碱氢氧化钠之间发生反应:SO2+OH-=HSO3-,NO和氢氧化钠之间不会反应,故答案为:SO2+OH-=HSO3-;
②甲烷燃料电池中,在碱性溶液中,甲烷燃料电池的负极反应式为CH4-8e-+10OH-═CO32-+7H2O,故每有1mol甲烷反应,转移电子数为8mol,每生成1molCe4+,提供电子为1mol,故答案为:8;
(2)①根据图象知,脱氢率越高越好,但Cr作催化剂时温度高于Mn,温度越高,对设备要求越高,增大生产成本,且脱氢率增大较小,所以使用Mn作催化剂较好;根据图象知,在温度为200-250℃或范围内间任意温度,脱氢率较高,故答案为:a;
②生成0.5mol氮气放出QkJ热量,则生成2mol氮气放出4QkJ热量,则其热化学反应方程式为2NH3(g)+NO(g)+NO2(g)?2N2(g)+3H2O(g)△H=-4QkJ/mol,
故答案为:2NH3(g)+NO(g)+NO2(g)?2N2(g)+3H2O(g)△H=-4QkJ/mol.
点评:本题重点考查图象的分析、热化学反应方程式的书写、原电池原理,注意原电池放电时,负极发生氧化反应,为易错点.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案
相关题目
下列说法中正确的是( )
| A、摩尔是表示物质质量的单位 |
| B、10g氟化氢含有0.5molHF分子 |
| C、1g氢气的物质的量是1mol |
| D、物质的摩尔质量等于其式量 |
下列说法或有关化学用语表达正确的是( )
| A、二氧化碳的结构式:O-C-O |
B、Cl-的结构示意图: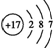 |
| C、乙醇的结构简式:CH3CH2OH |
| D、过氧化氢(D2O2)的相对分子质量为34 |
氮氧化物与悬浮在大气中海盐粒子的相互反应:4NO2(g)+2NaCl(s)═2NaNO3(s)+2NO(g)+Cl2(g),△H在恒温条件下,向2L恒容密闭容器中加入0.4mol NO2和0.2mol NaCl,10min反应达到平衡时n(NaNO3)=0.1mol,NO2的转化率为α.下列叙述中正确的是( )
| A、10min内NO浓度变化表示的速率v(NO)=0.01 mol?L-1?min-1 |
| B、若保持其他条件不变,在恒压下进行该反应,则平衡时NO2的转化率大于α |
| C、若升高温度,平衡逆向移动,则该反应的△H>0 |
| D、若起始时向容器中充入NO2(g) 0.1 mol、NO(g)0.2 mol和Cl2(g)0.1 mol(固体物质足量),则反应将向逆反应方向进行 |
理论上不能用于设计成原电池的反应是( )
| A、2H2(g)+O2(g)═2H2O(l)△H<0 |
| B、HCl(aq)+NaOH(aq)═NaCl(aq)+H2O(l)△H<0 |
| C、2Al(s)+3Cl2(g)═2AlCl3(s)△H<0 |
| D、Zn(s)+2HCl(aq)═ZnCl2+H2(g)△H<0 |