题目内容
2. 某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的准确浓度,现从市场上买来一瓶某品牌食用白醋,在实验室中用标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围:
某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的准确浓度,现从市场上买来一瓶某品牌食用白醋,在实验室中用标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围:| 指示剂 | 石蕊 | 甲基橙 | 甲基红 | 酚酞 |
| 变色范围(pH) | 5.0~8.0 | 3.1~4.4 | 4.4~6.2 | 8.2~10.0 |
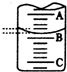
(2)如图表示50mL滴定管中液面的位置,若A与C刻度间相差1mL,A处的刻度为25,滴定管中液面读数应为25.40mL,此时滴定管中液体的体 积大于24.60ml.
(3)为了减小实验误差,该同学一共进行了三次实验,假设每次所取白醋体积均为VmL,NaOH标准液浓度为c mo1/L,三次实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液体积/mL | 26.02 | 25.35 | 25.30 |
A.实验结束时俯视滴定管中液面,读取滴定终点时NaOH溶液的体积
B.滴加NaOH溶液过快,未充分振荡,刚看到溶液变色,立刻停止滴定
C.盛装标准液的滴定管装液前用蒸馏水洗涤,未用标准液润洗
D.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
(4)根据所给数据,写出计算该白醋中醋酸的物质的量浓度的表达式(不必化简):c(CH3COOH)=$\frac{c×(25.35+25.30)}{2V}$mol/L.
分析 (1)精确量取酸性溶液应该用酸式滴定管;根据酸碱反应生成了强碱弱酸盐,溶液呈碱性,应选择碱性变色范围内的指示剂;通过观察溶液颜色变化判断终点,酚酞在酸性溶液中为无色,达到终点溶液稍显碱性,溶液变成浅红色;
(2)A与C刻度间相差1ml,说明每两个小格之间是0.1mL,A处的刻度为25,据此确定B的刻度,注意滴定管的上面数值小,下面数值大;又因为滴定管下面没有刻度,所以此时滴定管中液体的体积应大于50.00-25.40=24.60ml;
(3)根据所用过程判断不当操作对相关物理量的影响;
(4)根据化学方程式CH3COOH+NaOH═CH3COONa+H2O计算醋酸的浓度.
解答 解:(1)向锥形瓶中移取一定体积的白醋所用的仪器是酸式滴定管量取;醋酸与氢氧化钠反应生成了醋酸钠,醋酸钠属于强碱弱酸盐,溶液呈碱性,应选择碱性变色范围内的指示剂,故选酚酞;滴定时锥形瓶中为酸性溶液,酚酞在酸性溶液中为无色,达到终点溶液稍显碱性,变浅红色,则锥形瓶由无色变为浅红色且半分钟内不复原,说明达到滴定终点;
故答案为:酸式滴定管;酚酞;锥形瓶由无色变为浅红色且半分钟内不复原;
(2)A与C刻度间相差1ml,说明每两个小格之间是0.10mL,A处的刻度为25,A和B之间是四个小格,所以相差0.40mL,则B是25.40mL,又因为滴定管下面没有刻度,所以此时滴定管中液体的体积应大于50.00-25.40=24.60ml
故答案为:25.40;大于24.60ml;
(3)A.实验结束时俯视滴定管中液面,读取滴定终点时NaOH溶液的体积,液面偏高,读数偏小,导致NaOH溶液体积偏小,故A错误;
B.滴加NaOH溶液过快,未充分振荡,刚看到溶液变色,立刻停止滴定,反应不充分,导致NaOH溶液体积偏小,故B错误;
C.盛装标准液的滴定管装液前用蒸馏水润洗过,未用标准液润洗,标准液被稀释,浓度偏小,导致NaOH溶液体积偏大,故C正确;
D.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗,醋酸的物质的量偏大,导致NaOH溶液体积偏大,故D正确;
故选:CD;
(4)第一次数据相差较大,舍去,其余两次使用氢氧化钠溶液的平均体积=$\frac{25.35+25.30}{2}$mL,
CH3COOH+NaOH═CH3COONa+H2O
1 1
c(CH3COOH)×VmL cmo1/L×$\frac{25.35+25.30}{2}$mL
解得:c(CH3COOH)=$\frac{c×(25.35+25.30)}{2V}$mol/L;
故答案为:$\frac{c×(25.35+25.30)}{2V}$mol/L.
点评 本题主要考查了中和滴定操作、误差分析以及计算,难度不大,理解中和滴定的原理是解题关键.

 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案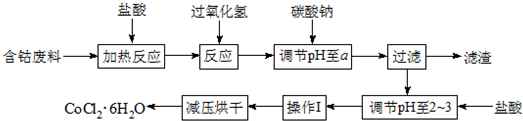
已知:
①钴与盐酸反应的化学方程式为:Co+2HCl→CoCl2+H2↑
②CoCl2•6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴.
③部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀 | 4.1 | 9.7 | 9.2 | 5.2 |
(2)加入碳酸钠调节pH至a,a的范围是5.2~7.6.
(3)操作Ⅰ包含3个实验基本操作,它们依次是蒸发浓缩、冷却结晶和过滤.
(4)制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解.
(5)为测定产品中CoCl2•6H2O含量,某同学将一定量的样品溶于水,再向其中加入足量的AgNO3溶液,过滤,并将沉淀烘干后称量其质量.通过计算发现产品中CoCl2•6H2O的质量分数大于100%,其原因可能是样品中含有NaCl杂质,CoCl2•6H2O烘干时失去了部分结晶水.
(6)在实验室,为了从上述产品中获得纯净的CoCl2•6H2O,通常先将产品溶解在乙醚中,除去不溶性杂质后,再进行蒸馏操作.
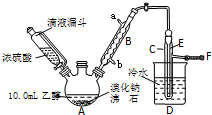 实验室用乙醇、浓硫酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):
实验室用乙醇、浓硫酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):H2SO4(浓)+NaBr$\frac{\underline{\;\;△\;\;}}{\;}$NaHSO4+HBr↑
CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O.有关数据见下表:
| 乙醇 | 溴乙烷 | 溴 | |
| 状态 | 无色液体 | 无色液体 | 深红色液体 |
| 密度/(g•cm-3) | 0.79 | 1.44 | 3.1 |
| 沸点/℃ | 78.5 | 38.4 | 59 |
(2)实验中用滴液漏斗代替分液漏斗的优点为平衡压强,使浓磷酸顺利流下
(3)氢溴酸与浓硫酸混合加热发生氧化还原的化学方程式为2HBr+H2SO4(浓)=Br2+SO2↑+2H2O
(4)加热A的目的是加快反应速率,蒸馏出溴乙烷,F接橡皮管导入稀NaOH溶液,其目的是吸收SO2、溴乙烷和溴蒸汽,防止防止空气污染.
(5)图中C中的导管E的末端须在水面以下,其原因是冷却并减少溴乙烷的挥发.
(6)将C中的馏出液转入锥形瓶中,边振荡边逐滴滴入浓H2SO41~2mL以除去水、乙醇等杂质,然后经过操作M,使经硫酸处理后的溴乙烷转入蒸馏瓶,加热蒸馏,收集到38~40℃的馏分约9.3g.
①操作M的名称为分液;为了控制38~40℃,加热使用水浴加热法
②从乙醇的角度考虑,本实验所得溴乙烷的产率是49.7%
(乙醇的相对分子质量为46,溴乙烷的相对分子质量为109)
I.配制100mL 0.10mol/L NaOH标准溶液.
II.取20.00mL待测稀盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准
NaOH溶液进行滴定.
III.重复上述滴定操作2~3次,记录数据如下.
| 实验 编号 | NaOH溶液的浓度(mol/L) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测HCl溶液的体积(mL) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |
(2)根据上述数据,可计算出该盐酸的浓度约为0.11mol/L(保留两位有效数字).
(3)排去碱式滴定管中气泡的方法应采用如图丙的操作,然后挤压玻璃球使尖嘴部分充满碱液.

(4)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有EF(多选扣分).
A.滴定终点读数时俯视读数 B.酸式滴定管使用前,水洗后未用待测盐酸润洗
C.锥形瓶水洗后未干燥 D.配制NaOH标准溶液时,没有等溶解液降至室温就转移至容量瓶中
E.配制NaOH标准溶液时,定容时仰视容量瓶的刻度线
F.碱式滴定管尖嘴部分有气泡,滴定后消失.
①这种错误操作不一定(填“一定”/“一定不”/“不一定”)会导致实验结果有误差.
②若按此法分别测定c(H+)相等的盐酸和醋酸溶液的pH,误差较大的是盐酸.
(2)用已知浓度的 NaOH 溶液测定某 HCl溶液的浓度,参考如图,从表中选出正确序号
| 序号 | 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 |  选用滴定管 |
| A | 碱 | 酸 | 石芯 | (乙) |
| B | 酸 | 碱 | 酚酞 | (甲) |
| C | 碱 | 酸 | 甲基橙 | (甲) |
| D | 酸 | 碱 | 酚酞 | (乙) |
A.配制标准溶液的氢氧化钠中混有Na2CO3杂质
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
E.未用标准液润洗碱式滴定管.
| A. | 电解过程中共转移0.4 mol电子 | B. | 原混合液中c(K+)为2.0 mol•L-l | ||
| C. | 电解得到的Cu的质量为6.4 g | D. | 电解后溶液中c(H+)为0.1 mol•L-l |
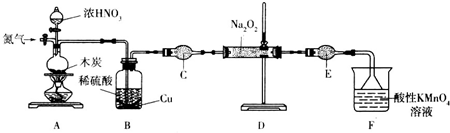
 某科研小组欲研究在其他条件不变的情况下,改变起始氧气的物质的量对合成新型硝化剂反应 4NO2(g)+O2(g)?2N2O5(g)△H<0的影响.
某科研小组欲研究在其他条件不变的情况下,改变起始氧气的物质的量对合成新型硝化剂反应 4NO2(g)+O2(g)?2N2O5(g)△H<0的影响.