题目内容
下列图示与对应的叙述相符的是( )
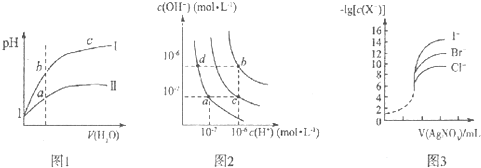

| A、图l表示同温度下,pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强 |
| B、图2中纯水仅升高温度,就可以从a点变到c点 |
| C、图2中在b点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显中性 |
| D、用0.0100 mol/L硝酸银标准溶液,滴定浓度均为0.1000 mol?L-1 Cl-、Br-及I-的混合溶液,由图3曲线,可确定首先沉淀的是Cl- |
考点:酸碱混合时的定性判断及有关ph的计算,水的电离,难溶电解质的溶解平衡及沉淀转化的本质
专题:图示题
分析:A、醋酸是弱电解质,在水溶液里存在电离平衡,加水稀释促进醋酸电离,溶液的导电性与溶液中离子浓度成正比;
B、仅升温促进水的电离,浓度和氢氧根离子浓度增大,氢离子浓度;和氢氧根离子浓度相同;
C、b点Kw=10-12,中性溶液pH=6;
D、-lg[c(X-)]的值越大,代表该离子的浓度越小.
B、仅升温促进水的电离,浓度和氢氧根离子浓度增大,氢离子浓度;和氢氧根离子浓度相同;
C、b点Kw=10-12,中性溶液pH=6;
D、-lg[c(X-)]的值越大,代表该离子的浓度越小.
解答:
解:A、醋酸是弱电解质,在水溶液里存在电离平衡,加水稀释促进醋酸电离,氯化氢是强电解质,完全电离,导致稀释过程中,醋酸中氢离子浓度大于盐酸,所以pH变化小的为醋酸,即II为醋酸,溶液的导电性与溶液中离子浓度成正比,a点导电能力大于b,故A错误;
B、仅升温促进水的电离,浓度和氢氧根离子浓度增大,氢离子浓度;和氢氧根离子浓度相同,与图象不相符合,故B错误;
C、b点Kw=10-12,中性溶液PH=6;将pH=2的硫酸与pH=10的NaOH溶液等体积混合后,氢离子浓度和氢氧根离子浓度相同,等体积混合溶液呈中性,故C正确;
D、-lg[c(X-)]的值越大,代表该离子的浓度越小,由图可知,加入一定量的硝酸银后I-的浓度最小,则I-首先沉淀,故D错误;
故选C.
B、仅升温促进水的电离,浓度和氢氧根离子浓度增大,氢离子浓度;和氢氧根离子浓度相同,与图象不相符合,故B错误;
C、b点Kw=10-12,中性溶液PH=6;将pH=2的硫酸与pH=10的NaOH溶液等体积混合后,氢离子浓度和氢氧根离子浓度相同,等体积混合溶液呈中性,故C正确;
D、-lg[c(X-)]的值越大,代表该离子的浓度越小,由图可知,加入一定量的硝酸银后I-的浓度最小,则I-首先沉淀,故D错误;
故选C.
点评:本题涉及知识点较多,这些知识点都是学习的难点,也是考试热点,根据弱电解质溶液中的电离平衡、盐的水解等知识来分析解答,题目难度中等.

练习册系列答案
相关题目
固氮是科学家致力研究的重要课题.自然界中存在天然的大气固氮过程:N2(g)+O2(g)═2NO (g)△H=+180.8kJ?mol-1工业合成氨则是人工固氮.分析两种固氮反应的平衡常数,下列结论正确的是( )
| 反应 | 大气固氮 | 工业固氮 | ||||
| 温度/℃ | 27 | 2000 | 25 | 350 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 4.1×106 | 1.847 | 0.507 | 0.152 |
| A、常温下,大气固氮很难进行,而工业固氮却容易进行 |
| B、模拟大气固氮应用于工业上的意义不大 |
| C、工业固氮时,温度越低时其K越大,所以温度越低反应速率越快 |
| D、大气固氮、工业固氮的反应都是放热反应 |
下列溶液中,跟100mL 0.5mol/L NaCl溶液所含的氯离子物质的量浓度相同的是( )
| A、100mL 0.5 mol/L MgCl2溶液 |
| B、25 mL 0.5mol/L HCl溶液 |
| C、50 mL 1mol/L NaCl溶液 |
| D、200 mL 0.25mol/L CaCl2溶液 |
下列各组物质中,物质之间通过一步反应就能实现图示转化的是( )
| 物质编号 | 物质转化关系 | a | b | c | d |
| ① | 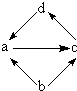 | FeCl2 | Fe | FeCl3 | CuCl2 |
| ② | Na2O | Na | Na2O2 | Mg(OH)2 | |
| ③ | NO | N2 | NO2 | NaCl | |
| ④ | Al2O3 | Al | Na[Al(OH)4] | Al(OH)3 |
| A、①②③ | B、①③④ |
| C、①④ | D、②④ |
 在25℃下,向10.00mL0.01mol?L-1某一元酸HA溶液中逐滴加入0,.01mol.L-1NaOH溶液,溶液pH变化曲线如图所示.下列说法正确的是( )
在25℃下,向10.00mL0.01mol?L-1某一元酸HA溶液中逐滴加入0,.01mol.L-1NaOH溶液,溶液pH变化曲线如图所示.下列说法正确的是( )| A、HA是强酸 |
| B、b点表示的溶液中:c(HA)=c(A-) |
| C、c点时:V=10.00mL |
| D、b、c、d三点表示的溶液中一定都存在:c(Na+)+c(H+)=c(A-)+c(OH-) |
下列叙述不正确的是( )
A、工业制H2SO4时,催化氧化阶段的反应原理为2SO2+O2
| ||||
B、海水提镁的主要步骤为 | ||||
C、冶炼铝时电解铝的反应原理为:2AlCl3
| ||||
D、高炉炼铁还原剂还原赤铁矿的化学方程式为:Fe2O3+3CO
|
2013年10月,三位美国化学家因为给复杂化学体系设计了多尺度模型而荣获诺贝尔化学奖.模型由C、H、O的两种或三种原子构成,有关说法错误的是( )
| 序号 | 1 | 2 | 3 | 4 |
| 模型示意图 |  |  |  |  |
| A、模型1对应的物质的二氯代物有2种 |
| B、模型2对应的物质的官能团是羧基 |
| C、模型2对应的物质与模型3对应的物质能发生酯化反应 |
| D、模型4对应的物质可以与氯气发生加成反应 |