题目内容
下列有关有机实验的叙述正确的是( )
| A、实验室制取乙烯时,应把无水乙醇与3mol/L的H2SO4混合均匀后迅速升温至170℃ |
| B、分馏操作中,温度计水银球应放置在蒸馏烧瓶支管口附近 |
| C、除去乙酸乙酯中乙酸杂质的方法是加入饱和NaOH溶液,充分振荡、静置后,分液 |
| D、检验溴乙烷中的湨元素的方法是加入NaOH溶液共热,冷却后滴入AgNO3溶液,观察有无浅黄色沉淀生成 |
考点:乙烯的实验室制法,溴乙烷的化学性质,蒸馏与分馏,物质的分离、提纯和除杂
专题:
分析:A.用乙醇与浓H2SO4混合共热到170℃制取乙烯,不能用稀硫酸;
B.温度计测量馏出物温度,则水银球应该放在蒸馏烧瓶的支管口处;
C.氢氧化钠溶液能够与乙酸乙酯反应,应该使用饱和碳酸钠溶液;
D.加入硝酸银溶液前需要加入稀硝酸中和氢氧化钠,否则影响银离子的检验.
B.温度计测量馏出物温度,则水银球应该放在蒸馏烧瓶的支管口处;
C.氢氧化钠溶液能够与乙酸乙酯反应,应该使用饱和碳酸钠溶液;
D.加入硝酸银溶液前需要加入稀硝酸中和氢氧化钠,否则影响银离子的检验.
解答:
解:A.用乙醇与浓H2SO4混合共热到170℃制取乙烯,浓硫酸作催化剂,3mol/L的H2SO4的浓度太小,故A错误;
B.分馏操作中,温度计用于测量馏出物温度,所以温度计水银球应放置在蒸馏烧瓶支管口附近,故B正确;
C.除去乙酸乙酯中乙酸杂质的方法是加入饱和碳酸钠溶液,充分振荡、静置后,分液,不能使用氢氧化钠溶液,否则乙酸乙酯在氢氧化钠溶液中发生水解,故C错误;
D.检验溴乙烷中的湨元素的方法是加入NaOH溶液共热,冷却后先用稀硝酸酸化,然后滴入AgNO3溶液,观察有无浅黄色沉淀生成,没有加入稀硝酸,原溶液中的氢氧化钠会干扰银离子检验,故D错误;
故选B.
B.分馏操作中,温度计用于测量馏出物温度,所以温度计水银球应放置在蒸馏烧瓶支管口附近,故B正确;
C.除去乙酸乙酯中乙酸杂质的方法是加入饱和碳酸钠溶液,充分振荡、静置后,分液,不能使用氢氧化钠溶液,否则乙酸乙酯在氢氧化钠溶液中发生水解,故C错误;
D.检验溴乙烷中的湨元素的方法是加入NaOH溶液共热,冷却后先用稀硝酸酸化,然后滴入AgNO3溶液,观察有无浅黄色沉淀生成,没有加入稀硝酸,原溶液中的氢氧化钠会干扰银离子检验,故D错误;
故选B.
点评:本题考查了常见化学实验基本操作方法、反应原理的判断,题目难度不大,试题侧重基础知识的考查,注意掌握常见反应原理、化学实验基本操作方法,试题有利于培养学生的分析、理解能力及灵活应用所学知识能力.

练习册系列答案
相关题目
有甲基、苯基、羟基、羧基两两结合(包括自身)的物质中,具有酸性的有机物种类有( )
| A、3种 | B、4种 | C、5种 | D、6种 |
可用来提取含有杂质Br2的溴苯的试剂是( )
| A、水 | B、酒精 |
| C、NaOH溶液 | D、苯 |

 (1)如图分别是温度计、量筒、滴定管的一部分,则:量筒应该是
(1)如图分别是温度计、量筒、滴定管的一部分,则:量筒应该是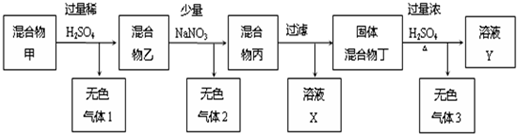
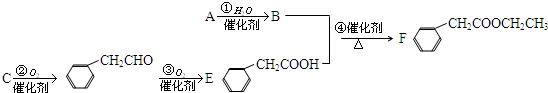
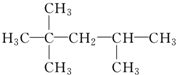 的名称是
的名称是