题目内容
1.下列表示方法或说法正确的是( )| A. | Na+的离子结构示意图: | |
| B. | 乙烯的结构简式为:CH2CH2 | |
| C. | 苯分子的结构中没有碳碳单键和碳碳双键,苯分子中的碳碳键是介于它们之间独特的键 | |
| D. | 实验室中用二氧化锰与稀盐酸反应制取Cl2 |
分析 A.钠离子核内有11个质子,核外有两个电子层,第一层两个电子,第二层八个电子;
B.乙烯的结构简式必须表示出碳碳双键;
C.苯分子含有一种特殊的化学键,键长介于C-C和C═C之间的独特的键;
D.实验室常用浓盐酸与二氧化锰反应来制取少量的氯气.
解答 解:A.钠离子核内有11个质子,核外有两个电子层,第一层两个电子,第二层八个电子,Na+的离子结构示意图: ,故A错误;
,故A错误;
B.乙酸结构简式应该为:CH2=CH2,故B错误;
C.苯分子含有一种特殊的化学键,键长介于C-C和C═C之间,不存在单纯的单、双键,故C正确;
D.实验室常用浓盐酸与二氧化锰反应来制取少量的氯气,稀盐酸不反应,故D错误.
故选C.
点评 本题考查常见化学用语的正误判断,题目难度中等,该题是高考中的常见题型与重要的考点,该题基础性强,难易适中,主要是考查学生对常见化学用语的熟悉掌握程度,该类试题需要明确的是常见的化学用语主要包括元素符号、化学式、化合价、电子式、原子结构示意图、结构式、结构简式以及方程式和各种模型等.

练习册系列答案
相关题目
11.用FeCl3酸性溶液脱除 H2S后的废液,通过控制电压电解得以再生.某同学使用石墨电极,在不同电压(x)下电解 pH=1 的 0.1mol/L FeCl2溶液,研究废液再生机理.记录如下(a、b、c代表电压值:)
(1)用 FeCl3酸性溶液脱除 H2S的离子方程式为2Fe3++H2S=2Fe2++2H++S↓.
(2)Ⅰ中,Fe3+产生的原因可能是 Cl- 在阳极放电,生成的 Cl2将 Fe2+氧化.写出有关反
应的方程式和电极反应式Cl2+2Fe2+=2Fe3++2Cl-;2Cl--2e-=Cl2↑.
(3)由Ⅱ推测,Fe3+产生的原因还可能是 Fe2+在阳极放电,电极反应式为Fe2+-e-=Fe3+.
(4)Ⅱ中虽未检测出 Cl2,但 Cl- 在阳极是否放电仍需进一步验证.电解 pH=1 的 NaCl溶液做对照实验,记录如下:
①NaCl溶液的浓度是0.2mol/L.
②与Ⅱ对比,可得出的结论:ABC
A.通过控制电压,验证了 Fe2+先于 Cl- 放 电
B.电压过小,Cl- 可 能 不 放 电
C. 通过控制电压,证实了产生 Fe3+的两种原因都成立
D. 通过控制电压,证实了产生 Fe3+一定仅是由于生成的 Cl2将 Fe2+氧化.
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| I | x≥a | 电极附近出现黄色,有气泡产生 | 有Fe3+、有Cl2 |
| II | a>x≥b | 电极附近出现黄色,无气泡产生 | 有Fe3+、无Cl2 |
| III | b>x>0 | 无明显变化 | 无Fe3+、无Cl2 |
(2)Ⅰ中,Fe3+产生的原因可能是 Cl- 在阳极放电,生成的 Cl2将 Fe2+氧化.写出有关反
应的方程式和电极反应式Cl2+2Fe2+=2Fe3++2Cl-;2Cl--2e-=Cl2↑.
(3)由Ⅱ推测,Fe3+产生的原因还可能是 Fe2+在阳极放电,电极反应式为Fe2+-e-=Fe3+.
(4)Ⅱ中虽未检测出 Cl2,但 Cl- 在阳极是否放电仍需进一步验证.电解 pH=1 的 NaCl溶液做对照实验,记录如下:
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅳ | a>x≥c | 无明显变化 | 有Cl2 |
| Ⅴ | c>x≥b | 无明显变化 | 无Cl2 |
②与Ⅱ对比,可得出的结论:ABC
A.通过控制电压,验证了 Fe2+先于 Cl- 放 电
B.电压过小,Cl- 可 能 不 放 电
C. 通过控制电压,证实了产生 Fe3+的两种原因都成立
D. 通过控制电压,证实了产生 Fe3+一定仅是由于生成的 Cl2将 Fe2+氧化.
9.在一定温度下的恒容的密闭容器中,当下列物理量不再发生变化时,反应A(g)+2B(g)?C(g)+D(g),不能表明已达到平衡状态的是( )
| A. | B物质的量浓度 | B. | 混合气体的密度 | ||
| C. | 混合气体的压强 | D. | 混合气体的平均相对分子量 |
16.某学生的实验报告所列出的下列数据中合理的是( )
| A. | 用10mL量筒量取7.13mL稀盐酸 | |
| B. | 用酸式滴定管量取25.00ml稀硫酸 | |
| C. | 用广泛pH试纸测得某溶液的pH为2.3 | |
| D. | 用托盘天平称量15.42gNaCl固体 |
6.下列叙述正确的是( )
| A. | 将40 g NaOH溶解于1 L水中,得到1 mol•L-1的NaOH溶液 | |
| B. | 将11.2 L HCl气体通入水配成0.5 L的溶液,浓度为1 mol•L-1 | |
| C. | 将1 L 10 mol•L-1的盐酸与9 L水混合,混合液浓度为1 mol•L-1 | |
| D. | 10 g NaOH溶解在水中配成250 mL溶液,其浓度为1 mol•L-1 |
11.元素周期表中碲元素的数据见下图,下列说法中正确的是( )


| A. | Te原子的相对原子质量是127.5 | |
| B. | Te元素可能会有多种同位素 | |
| C. | Te原子5p亚层有2对成对电子 | |
| D. | Te原子最外层有6个运动状态相同的电子 |
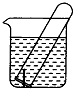 如图所示,水槽中试管内有一枚铁钉,放置数天观察:
如图所示,水槽中试管内有一枚铁钉,放置数天观察: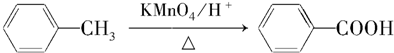

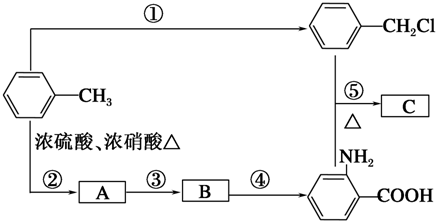
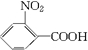 、A物质的结构简式是
、A物质的结构简式是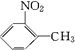 .
.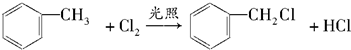 ,取代反应
,取代反应 ,取代反应.
,取代反应.