题目内容
10.下列陈述正确并且有因果关系的是( )| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | SO2有漂白性 | SO2可使溴水褪色 |
| B | Cl2有漂白性 | Cl2能使品红溶液褪色 |
| C | 浓硫酸有脱水性 | 浓硫酸可用于干燥H2和CO |
| D | Fe3+有强氧化性 | FeCl3溶液可用于回收废旧电路板中的铜 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.使溴水褪色体现了二氧化硫的还原性;
B.干燥Cl2本身不具有漂白性,能使品红溶液褪色,是由于氯气与水反应生成HClO的缘故;
C.浓硫酸具有吸水性故可用于干燥H2和CO;
D.Fe3+有强氧化性,可将铜氧化成铜离子,然后再还原出来.
解答 解:A.二氧化硫可使溴水褪色体现了还原性,故A错误
B.干燥Cl2本身不具有漂白性,能使品红溶液褪色,是由于氯气与水反应生成HClO的缘故,故B错误
C.浓硫酸可用于干燥H2和CO,是因为浓硫酸具有吸水性,故C错误;
D.FeCl3溶液可用于回收废旧电路板中的铜,是因为Fe3+有强氧化性,可将铜氧化成铜离子,然后再还原出来,故D正确;
故答案为:D.
点评 本题综合考查元素化合物知识,为高考常见题型,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
20.下列有关生铁和钢的说明正确的是( )
| A. | 生铁是混合物,钢是纯净物 | |
| B. | 用铁矿石来炼铁时,要加入如焦炭等氧化剂 | |
| C. | 不锈钢是铁和硅的合金,比纯铁硬度大,不易腐蚀 | |
| D. | 钢比生铁含碳量低 |
1.下列物质的包装上贴错了危险警告标签的是( )
| A. |  | B. |  | C. |  | D. |  |
18.N2和O2在一定条件下发生化合反应生成气体B,反应掉N2体积是反应掉O2体积的两倍(同温同压).则B分子的组成是( )
| A. | N2O | B. | NO | C. | NO2 | D. | N2O4 |
5.水溶液中能大量共存的一组离子是( )
| A. | NH4+、Ba2+、Brˉ、CO32ˉ | B. | Clˉ、NO3ˉ、Fe2+、H+ | ||
| C. | K+、Na+、SO42ˉ、MnO4ˉ | D. | Na+、H+、SO42ˉ、HCO3ˉ |
15.下列说法正确的是( )
| A. | 在100℃、101 kPa条件下,液态水的气化热为40.69 kJ•mol-1,则H2O(g)?H2O(l) 的△H=40.69 kJ•mol-1 | |||||||||||
| B. | Li、Be、B三种元素的第一电离能(I1)差别不大,而I2差别很大,则三种原子中最难失去第二个电子的是Be | |||||||||||
| C. | 已知:
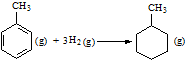 的△H为-384 kJ•mol-1 的△H为-384 kJ•mol-1 | |||||||||||
| D. | 固体NH5的所有原子的最外层均满足2个或8个电子的稳定结构,它与水反应的化学方程式为NH5+H2O═NH3•H2O+H2↑ |
2.下列变化中,需加入适当的还原剂才能完成的是( )
| A. | FeCl2→FeCl3 | B. | CuO→Cu | C. | KMnO4→MnO2 | D. | Cl2→NaCl |
19.某有机物的结构简式如图所示,下列有关物质的说法正确的是( )
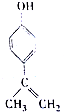

| A. | 该物质的分子式是C9H11O | |
| B. | 该物质分子中的所有C原子可以共面 | |
| C. | 滴入KMnO4(H+)溶液,可观察到紫色褪去,能证明结构中存在碳碳双键 | |
| D. | 1mol该物质分别与浓溴水和H2反应时,最多消耗Br2和H2分别是3mol、4mol |
20.下列除杂操作可行的是( )
| A. | 通过浓硫酸除去HCl中的H2O | |
| B. | 通过灼热的CuO除去H2中的CO | |
| C. | 通过灼热的镁粉除去CO2中的N2 | |
| D. | 通过饱和碳酸氢钠溶液除去Cl2中的HCl |