题目内容
18.下列说法正确的是( )| A. | 某气体通入品红溶液中,能使其褪色,则该气体为二氧化硫 | |
| B. | 向Fe(NO3)2溶液中滴加稀盐酸溶液变成黄色 | |
| C. | 某无色溶液中加入盐酸酸化的BaCl2溶液有白色沉淀生成,则原溶液中含有SO42- | |
| D. | 钠在空气中燃料产物为白色固体 |
分析 A.二氧化硫具有漂白性,但能使品红溶液褪色的不一定是二氧化硫;
B.向Fe(NO3)2溶液中滴加稀盐酸溶液,溶液中硝酸根离子在酸性溶液中形成稀硝酸具有强氧化性,能氧化亚铁离子;
C.某无色溶液中加入盐酸酸化的BaCl2溶液银离子也会生成白色沉淀;
D.钠在空气中燃烧生成淡黄色固体过氧化钠;
解答 解:A.某气体通入品红溶液中,能使其褪色,该气体可能为氯气、二氧化硫等氧化性气体,氯气和水反应生成的次氯酸具有漂白性,可以使品红溶液褪色,故A错误;
B.向Fe(NO3)2溶液中滴加稀盐酸溶液,溶液中硝酸根离子在酸性溶液中形成稀硝酸具有强氧化性,能氧化亚铁离子为铁离子,溶液变成黄色,故B正确;
C.某无色溶液中加入盐酸酸化的BaCl2溶液有白色沉淀生成,则原溶液中可能含有硫酸根离子或银离子,不能确定是否含硫酸根离子,故C错误;
D.钠在空气中燃烧生成淡黄色固体过氧化钠,2Na+O2$\frac{\underline{\;点燃\;}}{\;}$Na2O2,故D错误;
故选B.
点评 本题考查了物质性质、反应现象的分析判断,主要是二氧化硫、稀硝酸、离子检验、钠及其化合物性质,题目难度中等.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
18.下列应用或事实没有体现出胶体的性质的是( )
| A. | 在海水与河水交界处,已形成沙洲 | |
| B. | 清晨林间透过缕缕阳光 | |
| C. | 三氯化铁溶液中加入NaOH出现红褐色沉淀 | |
| D. | 向煮熟的豆浆里加入石膏或卤水以生产豆腐 |
19.下列各组有机物中,互为同分异构体的是( )
| A. |  | B. | 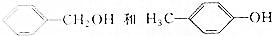 | ||
| C. |  | D. | 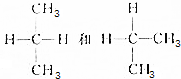 |
6.下列物质不属于既能跟盐酸反应又能跟NaOH溶液反应的是( )
| A. | Al | B. | Al2O3 | C. | Na2CO3 | D. | NaHCO3 |
13.实验室用足量Zn和100mL 4mol•L-1的H2SO4溶液制取H2,下列说法正确的是( )
| A. | 为提高反应速率,可换用98%的浓硫酸 | |
| B. | 在反应过程中,水的电离程度逐渐增大 | |
| C. | 在反应体系中加入硫酸钠溶液,反应速率不变 | |
| D. | 在反应体系中加入少量醋酸钠固体,反应速率变慢,生成氢气的量减少 |
3.现有25mL2mol•L-1的Na2CO3溶液和75mL1mol•L-1的稀盐酸.①将Na2CO3溶液缓慢滴到稀盐酸中;②将稀盐酸缓缓滴到Na2CO3溶液中,在标准状况下产生气体的体积情况是( )
| A. | 均为0.56 L | B. | ①=② | C. | ①>② | D. | ②>① |
7.铁及其化合物与生产、生活关系密切.

(1)如图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图.
①该电化腐蚀的类型为吸氧腐蚀.
②图中A、B、C三点附近的区域内,腐蚀最严重的是B(填字母).
(2)已知Fe3+、Fe2+、Cu2+在溶液中沉淀的pH如下表:
印刷电路铜板腐蚀剂常用FeCl3,腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10mol.L-1,请参照上表给出的数据和提供的药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤:①通入足量氯气;②加入CuO调节溶液的pH至3.2-4.7;③过滤.(提供的药品:Cl2、浓H2S04、NaOH溶液、CuO、Cu)
(3)用废铁皮制取铁红(Fe2O3)的部分流程示意图如图2:
①向Fe(NO3)2溶液中加入稀盐酸,溶液颜色由浅绿色变为棕黄色,该反应的原理为3Fe2++4H++NO3-=3Fe2++NO↑+2H2O(用离子方程式表示).
②步骤Ⅱ中发生反应:4Fe(NO3)2+O2+(2n+4)H2O═2Fe2O3•nH2O+8HNO3,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,结合流程写出该反应的化学方程式为4Fe+10HNO3═4Fe(NO3)2+NH4NO3+3H2O.
(4)某铁质容器材料为碳素钢,可盛装冷浓硫酸.取5.60g该材料放人15.0mL浓硫酸中加热,充分反应后得到溶液X并收集到气体Y.
①甲组通过实验确定了X中含有Fe3+,为检验X中是否还含有Fe2+,可另取X溶液加入BD(填序号).
A.KSCN溶液和氯水 B.K3[Fe(CN)6]溶液
C.NaOH溶液 D.酸性KMnO4溶液
②为分析气体Y中的成分,乙组将560mL(标准状况)气体Y通入足量溴水,然后向该溶液中加入足量BaCl2溶液,过滤、洗涤、干燥后,称得沉淀质量为2.33g.则气体Y通入足量溴水反应的离子方程式为SO2+Br2+2H2O=4H++2Br-+SO42-,参加该反应的气体在Y中的体积分数为40%.

(1)如图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图.
①该电化腐蚀的类型为吸氧腐蚀.
②图中A、B、C三点附近的区域内,腐蚀最严重的是B(填字母).
(2)已知Fe3+、Fe2+、Cu2+在溶液中沉淀的pH如下表:
| 阳离子 | Fe3+ | Fe2+ | Cu2+ |
| 开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 沉淀完全时的pH | 3.2 | 9.0 | 6.7 |
(3)用废铁皮制取铁红(Fe2O3)的部分流程示意图如图2:
①向Fe(NO3)2溶液中加入稀盐酸,溶液颜色由浅绿色变为棕黄色,该反应的原理为3Fe2++4H++NO3-=3Fe2++NO↑+2H2O(用离子方程式表示).
②步骤Ⅱ中发生反应:4Fe(NO3)2+O2+(2n+4)H2O═2Fe2O3•nH2O+8HNO3,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,结合流程写出该反应的化学方程式为4Fe+10HNO3═4Fe(NO3)2+NH4NO3+3H2O.
(4)某铁质容器材料为碳素钢,可盛装冷浓硫酸.取5.60g该材料放人15.0mL浓硫酸中加热,充分反应后得到溶液X并收集到气体Y.
①甲组通过实验确定了X中含有Fe3+,为检验X中是否还含有Fe2+,可另取X溶液加入BD(填序号).
A.KSCN溶液和氯水 B.K3[Fe(CN)6]溶液
C.NaOH溶液 D.酸性KMnO4溶液
②为分析气体Y中的成分,乙组将560mL(标准状况)气体Y通入足量溴水,然后向该溶液中加入足量BaCl2溶液,过滤、洗涤、干燥后,称得沉淀质量为2.33g.则气体Y通入足量溴水反应的离子方程式为SO2+Br2+2H2O=4H++2Br-+SO42-,参加该反应的气体在Y中的体积分数为40%.
8.分子式为C6H14的烷烃在结构式中含有3个甲基的同分异构体有多少( )
| A. | 2个 | B. | 3个 | C. | 4个 | D. | 5个 |
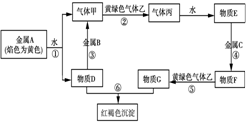 现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、红褐色沉淀H,已知黄绿色气体乙为Cl2,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出),请根据以上信息回答下列问题:
现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、红褐色沉淀H,已知黄绿色气体乙为Cl2,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出),请根据以上信息回答下列问题: