题目内容
在某温度下,将H2和I2各0.10mol的气态混合物充入l0L的密闭容器中,充分反应,达到平衡后,测得c(H2)=0.0080mol/L。则,氢气的转化率为 ;该温度下,反应的平衡常数为 ;已知该反应为放热反应,当降低温度时,反应的平衡常数会 (填“变大”、“变小”或“不变”)。
【答案】
( 6分) 20﹪ 0.25 变大 (各2分)
【解析】
试题分析:该反应的化学方程式是H2 + I2 2HI
2HI
起始浓度(mol/L) 0.01 0.01 0
转化浓度(mol/L) 0.002 0.002 0.004
平衡浓度(mol/L) 0.008 0.008 0.004
所以氢气的转化率是
该温度下,反应的平衡常数为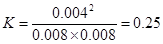
正反应是放热反应,则降低温度,平衡向正反应方向移动,平衡常数变大。
考点:考查可逆反应中转化率和平衡常数的计算以及外界条件对平衡常数的影响
点评:该题是中等难度的试题,该题也是高考中的重要考点和题型。该题基础性强,侧重能力的培养和解题方法的指导与训练,有助于培养学生的规范答题能力和逻辑推理能力。

练习册系列答案
相关题目