题目内容
18.下列分析及判断中正确的是( )| A. | 常温下0.1mol•L-1醋酸溶液pH=a,将溶液稀释到原体积的10倍pH=a+1 | |
| B. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012溶液中:NH4+、Al3+、NO3-、Cl-可以大量共存 | |
| C. | CO2分子中,碳氧键为极性键,正电荷中心和负电荷中心不重合,为极性分子 | |
| D. | pH=8.0的溶液中,CO2的主要存在形态为CO32- |
分析 A、醋酸溶液体积稀释10倍,pH值变化不到1个单位;
B、$\frac{c({H}^{+})}{c(O{H}^{-})}$=1012溶液呈酸性,酸性溶液中NH4+、Al3+、NO3-、Cl-可以大量共存;
C、CO2分子中,分子是直线型分子,正电荷中心和负电荷中心重合,为非极性分子;
D、pH=8.0的溶液中,是碱性溶液,CO2的主要存在形态为HCO3-.
解答 解:A、醋酸溶液体积稀释10倍,pH值变化不到1个单位,所以将溶液稀释到原体积的10倍pH<a+1,故A错误;
B、$\frac{c({H}^{+})}{c(O{H}^{-})}$=1012溶液呈酸性,酸性溶液中NH4+、Al3+、NO3-、Cl-可以大量共存,故B正确;
C、CO2分子中,分子是直线型分子,正电荷中心和负电荷中心重合,为非极性分子,不是极性分子,故C错误;
D、pH=8.0的溶液中,是碱性溶液,CO2的主要存在形态为HCO3-,而不是碳酸根离子,故D错误;
故选B.
点评 本题考查弱电解质的稀释、离子的共存、分子的极性和微粒的存在形式,综合性强,但难度不大.

练习册系列答案
相关题目
8.下列各组中属于同位素关系的是( )
| A. | ${\;}_{19}^{40}K$与${\;}_{20}^{40}Ca$ | B. | D2O与T2O | ||
| C. | ${\;}_{19}^{40}K$与${\;}_{19}^{39}K$ | D. | 白磷与红磷 |
3.下列烃形成的一氯代物种类最多的是( )
| A. | 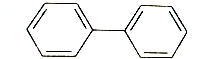 | B. | 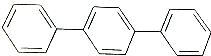 | ||
| C. | 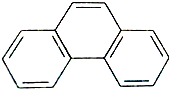 | D. | 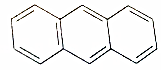 |
10.下列对相关有机物的描述不正确的是( )
| A. | 用灼烧的方法可以区分蚕丝和人造纤维 | |
| B. | 蛋白质遇重金属离子会变性 | |
| C. | α-氨基丙酸与α-氨基苯丙酸混合物脱水成肽,只生成2种二肽 | |
| D. | 食用油反复加热会产生稠环芳香烃等有害物质 |
7.设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
| A. | 标准状况下,2.24L苯中含有碳碳双键的数目为0.3NA | |
| B. | 标准状况下,22.4LC12与某物质充分反应,一定转移NA个电子 | |
| C. | 1L0.1mol•L-1的HF溶液中含有的分子数一定大于0.1NA | |
| D. | 含有10.7gFe(OH)3的氢氧化铁胶体中胶粒总数为0.1NA |
14.可逆反应A(g)+B(s)?C(g)+D(g)在恒温恒容的密闭容器中进行,下列选项中不能说明该反应已经达到平衡状态的是( )
| A. | 消耗amolA物质的同时消耗amolC物质 | |
| B. | 混合气体的质量不再改变 | |
| C. | B物质的浓度不再改变 | |
| D. | 容器内的压强不再改变 |
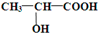
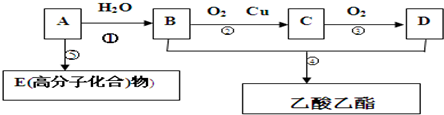
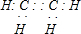
 CH3COOC2H5+H2O
CH3COOC2H5+H2O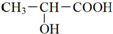 .在多种生物化学过程中乳酸起重要作用,在一般的新陈代谢和运动中乳酸不断被产生.请回答下列问题:
.在多种生物化学过程中乳酸起重要作用,在一般的新陈代谢和运动中乳酸不断被产生.请回答下列问题: