题目内容
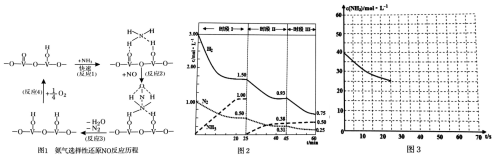
13. 工业上合成尿素(H2NCONH2)分为两步:
工业上合成尿素(H2NCONH2)分为两步:第一步,将液态氨气与气态CO2化合得到氨基甲酸铵(H2NCOONH4);
第二步,将氨基甲酸铵分解得到尿素:
H2NCOONH4(l)?H2O(1)+H2NCONH2 (1)△H1═+226.3kJ•mol-1.
(1)已知总反应的热化学方程式为:2NH3(l)+CO2(g)?H2O(1)+H2NCONH2 (1)△H2=-103.7kJ•mol-1.
①下列能提高尿素产率的措施是B.
A.升温 B.加压 C.添加催化剂
②写出第一步反应的热化学方程式2NH3(l)+CO2(g)?H2NCOONH4(l)△H=-330.0kJ•mol-1.
(2)已知:NH2COONH4(s)?2NH3(g)+CO2(g).某实验小组在一固定容积的密闭容器中加入NH2COONH4(s)进行实验,以探究外界因素对化学平衡移动的影响,记录了下列数据.
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度(×10-3mol•L-1) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
A.2v正(NH3)═v逆(CO2) B.密闭容器中氨气的体积分数不变
C.密闭容器中气体总浓度不变 D.混合气体的平均相对分子质量不变
②25.0℃与15.0℃时的平衡常数之比是8.
③上表实验的目的是探究温度对化学平衡的影响,通过数据分析得出的结论是升高温度平衡正向进行,正反应为吸热反应.
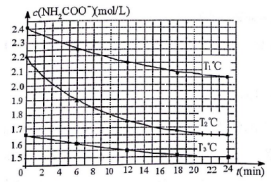
(3)已知:NH2COONH4+2H2O?NH4HCO3+NH3•H2O.该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图所示.
①计算T3℃时,0~12min氨基甲酸铵水解反应的平均速率0.0083mol/(L•min) (保留2位有效数字).
②比较图中T1、T2的大小:T1<T2(填“>”、“=”或“<”),判断的理由是T2℃反应物起始浓度比T1°C小,但相同时间内0-6min的平均反应速率仍比T1°C时的大.
分析 (1)①2NH3(l)+CO2(g)?H2O(1)+H2NCONH2 (1)△H2=-103.7kJ•mol-1,反应为气体体积减小的放热反应,提高尿素产率平衡正向进行;
②第一步,将液态氨气与气态CO2化合得到氨基甲酸铵(H2NCOONH4),结合热化学方程式和盖斯定律计算得到;
(2)①根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态;
②先根据反应 NH2COONH4(s)?2NH3(g)+CO2(g),可知平衡时容器内气体的浓度之比为2:1,由总浓度求出NH3、CO2 的平衡浓度,最后代入平衡常数的表达式来计算;
③上表实验的目的是探究温度对化学平衡的影响,升温平衡正向进行,向吸热反应方向进行;
(3)①根据化学反应速率的公式来计算;
②由图象数据可以得出,用不同初始浓度,不同温度下的平均速率的大小来说明.
解答 解:(1)①2NH3(l)+CO2(g)?H2O(1)+H2NCONH2 (1)△H2=-103.7kJ•mol-1,反应为气体体积减小的放热反应,提高尿素产率平衡正向进行,
A.升温平衡逆向进行,尿素产率减小,故A错误;
B.加压平衡正向进行,尿素产率增大,故B正确;
C.添加催化剂改变反应速率,不改变化学平衡,产率不变,故C错误;
故答案为:B;
②Ⅰ.H2NCOONH4(l)?H2O(1)+H2NCONH2 (1)△H1═+226.3kJ•mol-1,
Ⅱ.2NH3(l)+CO2(g)?H2O(1)+H2NCONH2 (1)△H2=-103.7kJ•mol-1,
盖斯定律计算Ⅱ-Ⅰ得到:2NH3(l)+CO2(g)?H2NCOONH4(l)△H=-330.0kJ•mol-1,
故答案为:2NH3(l)+CO2(g)?H2NCOONH4(l)△H=-330.0kJ•mol-1;
(2)①NH2COONH4(s)?2NH3(g)+CO2(g),反应为气体体积增大的反应,
A、2v正(NH3)═v逆(CO2) 未体现正逆的关系,v正(NH3)═2v逆(CO2)体现了正逆反应速率相同,故A错误;
B、因为反应物是固体,容器中氨气和二氧化碳的物质的量之比为2:1,密闭容器中氨气的体积分数不变,故B错误;
C、密闭容器中气体总浓度不变,说明总物质的量不变,正逆反应速率相等,故C正确;
D、因为反应物是固体,所以整个体系中气体摩尔质量是个定值,故D错误;
故答案为;C;
②25.0℃,总浓度为4.8×10-3 mol/L,容器内气体的浓度之比为2:1,故NH3和CO2的浓度分别为3.2×10-3 mol/L、1.6×10-3 mol/L,代入平衡常数表达式:K=(3.2×10-3)2×1.6×10-3 =1.6384×10-8,
15.0℃时,总浓度为2.4×10-3 mol/L,容器内气体的浓度之比为2:1,故NH3和CO2的浓度分别为1.6×10-3 mol/L、0.8×10-3 mol/L,代入平衡常数表达式:K=(1.6×10-3)2×0.8×10-3 =2.048×10-9,25.0℃与15.0℃时的平衡常数之比=1.6384×10-8:2.048×10-9=8,
故答案为:8;
(3)T3℃时,0~12min氨基甲酸铵水解反应的平均速率,依据图象可知浓度变化c(NH2COO-)=1.65mol/L-1.1.55mol/L=0.1mol/L,化学反应速率V=$\frac{0.1mol/L}{12min}$=0.0083mol/(L•min),
故答案为:0.0083mol/(L•min);
⑤因T2℃反应物起始浓度较小,但0~6min的平均反应速率(曲线的斜率)仍比T1℃大,说明T1<T2,T2℃反应物起始浓度比T1°C小,但相同时间内0-6min的平均反应速率仍比T1°C时的大,
故答案为:<;T2℃反应物起始浓度比T1°C小,但相同时间内0-6min的平均反应速率仍比T1°C时的大.
点评 本题考查了热化学方程式书写、化学平衡状态的判断、平衡常数的计算,反应速率的计算、图象分析应用等,注重了基础知识的考查,题目难度中等.

 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案| A. | 乙烷、乙烯、乙炔都难溶于水,且密度比水小 | |
| B. | 可用溴水来鉴别乙烷、乙烯和乙炔三种无色气体 | |
| C. | 在一定条件下,乙烷、乙烯、乙炔都能与氯气发生同类型反应 | |
| D. | 乙烷、乙烯、乙炔都能发生加聚反应生成高分子化合物 |
| A. | 浓氨水、浓硝酸应保存在棕色试剂瓶中,并置于阴凉处 | |
| B. | 液溴易挥发,应保存在棕色试剂瓶中,并加水封 | |
| C. | 在储存铵态化肥时,应密封包装并放在阴凉通风处 | |
| D. | 碘易升华,应保存在棕色细口瓶中,并置于阴凉处 |
| A. | 取等体积、pH相同的醋酸和盐酸分别稀释至原溶液的m倍和n倍,结果两溶液的pH仍然相同,则m<n | |
| B. | 将pH=2的CH3COOH溶液加水稀释,水的电离平衡也向右移动 | |
| C. | 常温下,将pH=2的H2SO4与pH=12的NH3•H2O溶液等体积混合后,混合液pH<7 | |
| D. | 某温度下水的离子积为1×10-12,若使pH=1的H2SO4与pH=12的NaOH溶液混合后溶液呈中性,则两者的体积比为1:10 |
| A. | 加入酚酞呈红色的溶液中:CO32-、NH4+、NO3-、K+ | |
| B. | 含有大量NO3-的溶液中:H+、Na+、Fe2+、Cl- | |
| C. | 强酸性溶液中:Fe3+、NH4+、Cl-、SCN- | |
| D. | 含有NaHSO4的溶液中:K+、Cu2+、Cl-、NO3- |
| A. | NaOH | B. | H2SO4 | C. | SO2 | D. | NaCl |
| A. |  氢燃料电池 | B. |  锌锰碱性电池 | C. |  铅蓄电池 | D. |  银锌纽扣电池 |