题目内容
A、B、C、D、E是元素周期表中的短周期主族元素,且原子序数依次增大.已知A与B不在同周期,A与C同主族,B原子最外层电子数是其电子层数的2倍,A、C、E原子最外层电子数之和为6,D的氧化物具有两性.下列说法正确的是( )
| A、A、B只能形成一种化合物 |
| B、离子半径:C<D |
| C、气态氢化物的稳定性:B>E |
| D、元素C、D的最高价氧化物对应水化物之间不能发生反应 |
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A、B、C、D、E是元素周期表中的短周期主族元素,且原子序数依次增大,D的氧化物具有两性,则D是Al元素;
B原子最外层电子数是其电子层数的2倍,最外层电子数不超过8,B的原子序数小于D,则B为C元素;
A与B不在同周期,A与C同主族,A的原子序数小于B,则A是H元素;
A和C属于同主族,且C的原子序数大于B而小于D,所以C是Na元素;
A、C、E原子最外层电子数之和为6,则E是Si元素,
再结合元素周期律解答.
B原子最外层电子数是其电子层数的2倍,最外层电子数不超过8,B的原子序数小于D,则B为C元素;
A与B不在同周期,A与C同主族,A的原子序数小于B,则A是H元素;
A和C属于同主族,且C的原子序数大于B而小于D,所以C是Na元素;
A、C、E原子最外层电子数之和为6,则E是Si元素,
再结合元素周期律解答.
解答:
解:A、B、C、D、E是元素周期表中的短周期主族元素,且原子序数依次增大,D的氧化物具有两性,则D是Al元素;
B原子最外层电子数是其电子层数的2倍,最外层电子数不超过8,B的原子序数小于D,则B为C元素;
A与B不在同周期,A与C同主族,A的原子序数小于B,则A是H元素;
A和C属于同主族,且C的原子序数大于B而小于D,所以C是Na元素;
A、C、E原子最外层电子数之和为6,则E是Si元素,
A.A、B能形成烃类化合物,所以有多种,故A错误;
B.C是Na元素、D是Al元素,电子层结构相同的离子,其离子半径随着原子序数增大而减小,所以离子半径:C>D,故B错误;
C.元素的非金属性越强,其气态氢化物越稳定,C元素的非金属性大于Si元素,所以气态氢化物的稳定性:B>E,故C正确;
D.元素C、D的最高价氧化物对应水化物分别是NaOH、Al(OH)3,二者能反应生成偏铝酸钠和水,故D错误;
故选C.
B原子最外层电子数是其电子层数的2倍,最外层电子数不超过8,B的原子序数小于D,则B为C元素;
A与B不在同周期,A与C同主族,A的原子序数小于B,则A是H元素;
A和C属于同主族,且C的原子序数大于B而小于D,所以C是Na元素;
A、C、E原子最外层电子数之和为6,则E是Si元素,
A.A、B能形成烃类化合物,所以有多种,故A错误;
B.C是Na元素、D是Al元素,电子层结构相同的离子,其离子半径随着原子序数增大而减小,所以离子半径:C>D,故B错误;
C.元素的非金属性越强,其气态氢化物越稳定,C元素的非金属性大于Si元素,所以气态氢化物的稳定性:B>E,故C正确;
D.元素C、D的最高价氧化物对应水化物分别是NaOH、Al(OH)3,二者能反应生成偏铝酸钠和水,故D错误;
故选C.
点评:本题考查了元素位置结构性质的相互关系及应用,根据元素周期表及原子结构确定元素,再结合元素周期律解答,知道氢氧化铝的两性,非金属性强弱的判断方法,题目难度不大.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
相同物质的量的O2和O3一定具有相同的( )
| A、原子数 | B、分子数 |
| C、体积 | D、质量 |
分别向下列各溶液中加入少量NaOH固体,溶液的导电能力变化不大的是 ( )
| A、自来水 |
| B、NaCl溶液 |
| C、醋酸溶液 |
| D、HCl溶液 |
对可逆反应:N2+3H2?2NH3达平衡时,若分别增大压强和降低压强,两种情况下对平衡体系正逆反应速率影响较大的依次是( )
| A、正反应速率,正反应速率 |
| B、逆反应速率,逆反应速率 |
| C、正反应速率,逆反应速率 |
| D、逆反应速率,正反应速率 |
下列各组物质的反应,能用H++OH-=H2O表示的是( )
| A、硫酸和氢氧化钡溶液 |
| B、盐酸和烧碱溶液 |
| C、硫酸和氢氧化铜 |
| D、盐酸和氢氧化铁 |
漆酚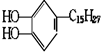 ,若涂在物体表面,在空气中干燥时会产生黑色漆膜,则漆酚不具有的化学性质是( )
,若涂在物体表面,在空气中干燥时会产生黑色漆膜,则漆酚不具有的化学性质是( )
 ,若涂在物体表面,在空气中干燥时会产生黑色漆膜,则漆酚不具有的化学性质是( )
,若涂在物体表面,在空气中干燥时会产生黑色漆膜,则漆酚不具有的化学性质是( )| A、可与烧碱溶液反应 |
| B、可与溴水发生取代反应 |
| C、可与酸性高锰酸钾溶液反应 |
| D、可与碳酸氢钠溶液反应放出二氧化碳 |
下列表示对应化学反应的离子方程式正确的是( )
| A、用过量NaOH溶液吸收SO2:OH-+SO2=HSO3- |
| B、Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O |
| C、Fe3O4溶于稀盐酸:Fe3O4+8H+=3Fe2++4H2O |
| D、NaHSO4溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
已知:11P4(白磷)+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4,若有9 mol的CuSO4参加反应,则被硫酸铜氧化的白磷分子的物质的量为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列各组离子在溶液中可以大量共存的是( )
| A、H+.CO32-.NO3-.SO42- |
| B、Ba2+.Cl-.NO3-.CO32- |
| C、Cu2+.H+.SO42-.Cl- |
| D、Ag+.OH-.CO32-.H+ |