题目内容
(6分)在标准状况下,用一定量的水吸收氨气后得到浓度为12.0 mol/L密度为0.915g·cm-3的氨水,试计算(要求写出计算过程):
(1)该氨水溶质的质量分数ω是多少?(用百分数表示,保留到小数点后一位数)
(2)1 L水吸收标准状况下的氨气多少升可制得上述氨水?(水的密度以1.00g·cm-3计,计算结果取整数。)
(6分)
【解析】
(1)该氨水溶质的质量分数ω为:
ω=C×M/(1000×ρ)=12×17/(1000×0.915)=0.223=22.3% (3分)
(2) 设吸收X L体积的NH3
则c=(X/22.4)/[ (1000+17X/22.4)/(0.915×1000)]=915X/(22400+17X)=12
x=378 L (3分)
【解析】
试题分析:(1)由c=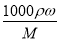 得ω=C×M/(1000×ρ)代入数据得12×17/(1000×0.915)=0.223=22.3%
得ω=C×M/(1000×ρ)代入数据得12×17/(1000×0.915)=0.223=22.3%
(2) 设吸收X L的NH3 则NH3的物质的量为X/22.4mol 溶液的质量为17X/22.4+1000g ,溶液的体积为(17X/22.4+1000)g/(0.915g·cm-3×1000)L,可知c=(X/22.4)/[ (1000+17X/22.4)/(0.915×1000)]=12mol/L ,解得x=378L 。
考点:物质的量浓度与质量分数的关系

练习册系列答案
相关题目