��Ŀ����
���Ե缫���NaCl��Һ��CuSO4��Һ���õ����ֲ���A��B��C��������֮���ת����ϵ����ͼ��ʾ��ͼ�в��뷴Ӧ�����ɵ�ˮ������ȥ������֪���Ƕ�����Ԫ�صĵ��ʣ������ճ������г��õİ�װ���ϡ�

�ش��������⣺
����������NaCl��Һ��
�ټ���A��Ӧ�Ļ�ѧ����ʽ������ �������������� ��
��A��B��Ӧ�����ӷ���ʽ������ ������������ ����
�������100mL0.1 mol��L��1NaCl��Һ������������������112mL���壨��״��������������Һ��pHΪ���������������Է�Ӧǰ����Һ������仯����������ˮ��Ӱ�죩��
����������CuSO4��Һ��
��E�Ļ�ѧʽ�� �����ʱ�����ĵ缫��Ӧʽ������ ��
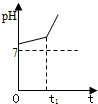
�ڼ���ʱ��A��Ũ��Һ����B������Ӧ��A��Ũ����ʱ��仯��ͼ����ȷ�� ��

���𰸡���10�֣�
�Ţ�2Al+ 2NaOH +2H2O = 2NaAlO2 + 3H2����������2�֣�
�� Cl2��2OH��= Cl��+ClO��+H2O��������2�֣� �� 13 ���� ��2�֣�
�Ƣ�SO2������1�֣� 4OH����4e����O2����2H2O��������3�֣�
��A������1�֣�����
�������������NaCl��Һ��������Һ�Լ��ԣ������CuSO4��Һ��������Һ�����ԣ����ڵ��ʼ���2�������¾�������H2���ʼ���Al���������NaCl��Һ�����ʱ���ܷ�Ӧ����ʽΪ2NaCl+2H2O![]() 2NaOH+H2��+Cl2������A��NaOH��B��Cl2��C��H2��������������������112mL����ʱ������NaOH0.01 mol����Һ��c(NaOH)=0.1 mol��L��1������Һ��pH=13���������CuSO4��Һʱ�����ʱ���ܷ�ӦʽΪ2CuSO4+2H2O
2NaOH+H2��+Cl2������A��NaOH��B��Cl2��C��H2��������������������112mL����ʱ������NaOH0.01 mol����Һ��c(NaOH)=0.1 mol��L��1������Һ��pH=13���������CuSO4��Һʱ�����ʱ���ܷ�ӦʽΪ2CuSO4+2H2O![]() 2H2SO4+O2��+2Cu����A��H2SO4��B��Cu��C��O2��E��SO2��A��Ũ��Һ��B��Ӧ�Ļ�ѧ����ʽΪCu+2H2SO4(Ũ)
2H2SO4+O2��+2Cu����A��H2SO4��B��Cu��C��O2��E��SO2��A��Ũ��Һ��B��Ӧ�Ļ�ѧ����ʽΪCu+2H2SO4(Ũ)![]() CuSO4+SO2��+2H2O������ϡ�����ͭ����Ӧ���κ�һ����Ӧ�������ٵ�2��������֪ѡ��A��ȷ��
CuSO4+SO2��+2H2O������ϡ�����ͭ����Ӧ���κ�һ����Ӧ�������ٵ�2��������֪ѡ��A��ȷ��
�����㡿Ԫ�ؼ��仯����绯ѧ����

 �¿α�ͬ��ѵ��ϵ�д�
�¿α�ͬ��ѵ��ϵ�д� һ����ʦ����Ӧ����������һ��ȫϵ�д�
һ����ʦ����Ӧ����������һ��ȫϵ�д�����˼ά�ǻ�ѧ�����г��õ�һ��˼ά�����������й����ӷ���ʽ��������ȷ���ǣ�������
|
��2010?��ƽ��ģ�⣩�±��Գ��������ȷ�Լ������������ϵ���ж϶���ȷ���ǣ�������
|
 ��1�������£���pH=6������ˮ�м���2.3g�����ƣ���ַ�Ӧ���ټ�����ˮϡ�͵�1L��������Һ��pH=
��1�������£���pH=6������ˮ�м���2.3g�����ƣ���ַ�Ӧ���ټ�����ˮϡ�͵�1L��������Һ��pH=