题目内容
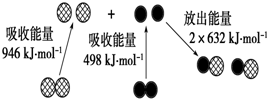 (1)化学反应中的能量变化,是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同所致.如图为N2(g)和O2(g)生成NO (g)过程中的能量变化:
(1)化学反应中的能量变化,是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同所致.如图为N2(g)和O2(g)生成NO (g)过程中的能量变化:①人们通常把拆开1mol某化学键所吸收的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,则N≡N键的键能为
②根据NO(g)分解生成N2(g)和O2(g)的热化学方程式,当有16g O2(g)生成时,该反应中放出的热量为
(2)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S.已知:
①CO(g)+
| 1 |
| 2 |
②S(s)+O2(g)═SO2(g)△H=-296.0kJ?mol-1
此反应的热化学方程式是
考点:有关反应热的计算
专题:化学反应中的能量变化
分析:(1)①根据拆开1mol某化学键所吸收的能量看成该化学键的键能,结合图示即可解答;根据反应热等于反应物的总键能减去生成物的总键能计算;
②根据热化学方程式热量与质量成正比;
(2)利用盖斯定律进行书写;
②根据热化学方程式热量与质量成正比;
(2)利用盖斯定律进行书写;
解答:
解:(1)由图可知:N≡N键的键能为946kJ?mol-1,反应热为946kJ?mol-1+498kJ?mol-1-2×632kJ?mol-1=180 kJ?mol-1,热化学方程式为:N2(g)+O2(g)═2NO(g)△H=+180 kJ?mol-1;
故答案为:946;N2(g)+O2(g)═2NO(g)△H=+180 kJ?mol-1;
(2)由N2(g)+O2(g)═2NO(g)△H=+180 kJ?mol-1可知当有16g O2(g)(即0.5mol)生成时,该反应中放出的热量为90kJ;
故答案为:90;
(3)①CO(g)+
O2(g)=CO2(g)△H=-283.0KJ?mol-1
②S(s)+O2(g)=SO2(g)△H=-296.0KJ?mol-1
将方程式①×2-②得2CO(g)+SO2(g)=S(s)+2CO2(g)△H=(-283.0KJ?mol-1)×2-(-296.0KJ?mol-1)=-270KJ?mol-1,热化学反应方程式为:2CO(g)+SO2(g)=S(s)+2CO2(g)△H=-270KJ?mol-1,
故答案为:2CO(g)+SO2(g)=S(s)+2CO2(g)△H=-270KJ?mol-1;
故答案为:946;N2(g)+O2(g)═2NO(g)△H=+180 kJ?mol-1;
(2)由N2(g)+O2(g)═2NO(g)△H=+180 kJ?mol-1可知当有16g O2(g)(即0.5mol)生成时,该反应中放出的热量为90kJ;
故答案为:90;
(3)①CO(g)+
| 1 |
| 2 |
②S(s)+O2(g)=SO2(g)△H=-296.0KJ?mol-1
将方程式①×2-②得2CO(g)+SO2(g)=S(s)+2CO2(g)△H=(-283.0KJ?mol-1)×2-(-296.0KJ?mol-1)=-270KJ?mol-1,热化学反应方程式为:2CO(g)+SO2(g)=S(s)+2CO2(g)△H=-270KJ?mol-1,
故答案为:2CO(g)+SO2(g)=S(s)+2CO2(g)△H=-270KJ?mol-1;
点评:本题考查综合考查化学反应与能量变化知识,注意键能与反应热的计算关系,题目难度中等

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
第三周期元素(不包括稀有气体),随着原子序数的递增,下列说法不正确的是( )
| A、最外层电子数逐渐增多 |
| B、原子半径逐渐减小 |
| C、简单离子半径逐渐减小 |
| D、元素的最高化合价逐渐增加 |
甲苯和丙三醇以一定比例混合,测得混合物含碳51.3%,那么氧元素的质量分数是( )
| A、40% | B、35% |
| C、30% | D、无法计算 |
下列物质①乙烷 ②丙烷 ③乙醇,沸点由高到低的顺序正确的是( )
| A、①>②>③ |
| B、②>①>③ |
| C、③>②>① |
| D、③>①>② |
煤燃烧的烟气中含有CO和SO2气体,下列关于这两种气体的说法正确的是( )
| A、两者都易溶于水 |
| B、两者都是有毒气体 |
| C、两者都能使品红溶液褪色 |
| D、两者都是形成酸雨的主要原因 |

 如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题: