题目内容
7.常温下,下列各组离子一定能在指定溶液中大量共存的是( )| A. | 投入足量漂白粉后的溶液中:Fe2+、H+、Cl-、SO42- | |
| B. | 0.1mol/LFeCl3溶液中:Na+、Ba2+、NO3-、SCN- | |
| C. | $\frac{{K}_{w}}{c({H}^{+})}$=1×10-13mol/L的溶液中:NH4+、Ca2+、Cl、NO3- | |
| D. | 水电离的c(OH-)=1×10-13mol/L的溶液中:K+、Na+、AlO2-、CO32- |
分析 A.投入足量漂白粉后的溶液,具有氧化性;
B.离子之间结合生成络离子;
C.$\frac{{K}_{w}}{c({H}^{+})}$=1×10-13mol/L的溶液,显酸性;
D.水电离的c(OH-)=1×10-13mol/L的溶液,为酸或碱溶液.
解答 解:A.投入足量漂白粉后的溶液,具有氧化性,与Fe2+发生氧化还原反应,不能共存,故A错误;
B.Fe3+、SCN-结合生成络离子,不能共存,故B错误;
C.$\frac{{K}_{w}}{c({H}^{+})}$=1×10-13mol/L的溶液,显酸性,该组离子之间不反应,可大量共存,故C正确;
D.水电离的c(OH-)=1×10-13mol/L的溶液,为酸或碱溶液,酸溶液中不能大量存在AlO2-、CO32-,故D错误;
故选C.
点评 本题考查离子共存,为高频考点,把握习题中的信息及离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应、氧化还原反应的判断,题目难度不大.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
17.下列相关反应的离子方程式书写正确的是( )
| A. | 用小苏打治疗胃酸过多:CO32-+2H+=CO2↑+H2O | |
| B. | 稀硝酸中加入过量的铁粉:Fe+4H++NO3-=Fe2++NO↑+2H2O | |
| C. | Ba(HCO3)2溶液中加入过量的NaOH溶液:2HCO3-+Ba2++2OH-=BaCO3↓+2H2O+CO32- | |
| D. | 用惰性电极电解饱和氯化镁溶液:2Cl-+2H2O $\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑ |
18.一氧化氮对空气说:一看到你我就会脸红,可逆反应2NO(g)+O2(g)?2NO2(g) 达到平衡状态时的标志是( )
| A. | 混合气体的密度不变 | |
| B. | 混合气体的颜色不再改变 | |
| C. | 正反应速率与逆反应速率相等均为零 | |
| D. | 反应物与生成物浓度相等 |
15.已知1g氢气完全燃烧生成水蒸气时,放出热量121kJ.且氢气中1mol H-H键断裂时吸收热量为436kJ,水蒸气中1mol H-O键形成时放出热量463kJ,则破坏1mol氧氧间的共价键需要吸收的热量为( )
| A. | 932kJ | B. | 859 kJ | C. | 538 kJ | D. | 496kJ |
12.以废旧铅酸电池中的含铅废料(Pb、PbO、PbO2、PbSO4及炭黑等)为原料,制备粗铅,实现铅的再生利用.其工作流程如1所示:
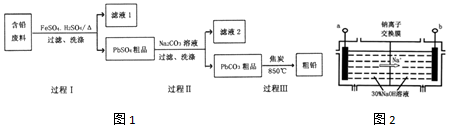
已知:Ksp(PbSO4)=1.6×10-5,Ksp(PbCO3)=3.3×10-14.
(1)过程I中,在Fe2+催化下,Pb和PbO2反应生成PbSO4的化学方程式是Pb+PbO2+2H2SO4$\frac{\underline{\;Fe_{2}+\;}}{\;}$2PbSO4+2H2O.
(2)过程I中,Fe2+催化过程可表示为:
i.2Fe2++PbO2+4H++SO42-═2Fe3++PbSO4+2H2O
ii.….
①写出ii的离子方程式:2Fe3++Pb+SO42-=PbSO4+2Fe2+;
②下列实验方案可证实上述催化过程.将实验方案补充完整.
(3)过程Ⅱ的目的是脱硫.若滤液2中c(SO42-)=1.6mol•L-1,c(CO32-)=0.1mol•L-1,则PbCO3中否(填“是”或“否”)混有PbSO4.
(4)钠离子交换膜固相电解法是从含铅废料中提取铅的一种新工艺,其装置如图2所示.将含铅废料投入阴极室,含铅废料中的PbSO4与NaOH溶液发生反应:PbSO4+3OH-═HPbO2-+SO42-+H2O.
①b与外接电源的负极相连;
②电解过程中,PbO2、PbO、HPbO2-在阴极放电,其中PbO2放电的电极反应式为PbO2+4e-+2H2O=Pb+4OH-;
③与传统无膜固相电解法相比,使用钠离子交换膜可以提高Pb元素的利用率,原因是阻止HPbO2-进入阳极室被氧化.

已知:Ksp(PbSO4)=1.6×10-5,Ksp(PbCO3)=3.3×10-14.
(1)过程I中,在Fe2+催化下,Pb和PbO2反应生成PbSO4的化学方程式是Pb+PbO2+2H2SO4$\frac{\underline{\;Fe_{2}+\;}}{\;}$2PbSO4+2H2O.
(2)过程I中,Fe2+催化过程可表示为:
i.2Fe2++PbO2+4H++SO42-═2Fe3++PbSO4+2H2O
ii.….
①写出ii的离子方程式:2Fe3++Pb+SO42-=PbSO4+2Fe2+;
②下列实验方案可证实上述催化过程.将实验方案补充完整.
| 编号 | 实验操作 | 现象 |
| 步骤1 | 向酸化的FeSO4溶液中加入KSCN溶液 | 溶液几乎无色 |
| 步骤2 | 取步骤1中反应液少量,加入少量PbO2,充分反应 | 溶液变红 |
| 步骤3 | 取步骤2中反应液少量,加入足量Pb,充分反应 | 红色褪去 |
(4)钠离子交换膜固相电解法是从含铅废料中提取铅的一种新工艺,其装置如图2所示.将含铅废料投入阴极室,含铅废料中的PbSO4与NaOH溶液发生反应:PbSO4+3OH-═HPbO2-+SO42-+H2O.
①b与外接电源的负极相连;
②电解过程中,PbO2、PbO、HPbO2-在阴极放电,其中PbO2放电的电极反应式为PbO2+4e-+2H2O=Pb+4OH-;
③与传统无膜固相电解法相比,使用钠离子交换膜可以提高Pb元素的利用率,原因是阻止HPbO2-进入阳极室被氧化.
19.下列有关说法正确的是( )
| A. | 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 | |
| B. | 古代做衣服的主要原料麻,其主要成分可表示为(C6H12O6)n | |
| C. | 稀豆浆、硅酸、氯化铁溶液均为胶体 | |
| D. | 食盐中含适量的碘酸钾,食用后可有效地抗核辐射 |
16.“嫦娥一号”需完成的四大科学目标之一是探测下列14种元素K、Th、U、O、Si、Mg、Al、Ca、Fe、Ti、Na、Cr、Cd在月球的含量和分布,其中属于短周期元索的有( )
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
17.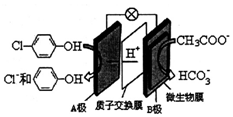 利用原电池原理除去废水中的乙酸钠和对氯酚(
利用原电池原理除去废水中的乙酸钠和对氯酚(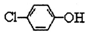 ),其原理如图所示,下列说法不正确的是( )
),其原理如图所示,下列说法不正确的是( )
 利用原电池原理除去废水中的乙酸钠和对氯酚(
利用原电池原理除去废水中的乙酸钠和对氯酚( ),其原理如图所示,下列说法不正确的是( )
),其原理如图所示,下列说法不正确的是( )| A. | 电流方向从A极沿导线流向B极 | |
| B. | 每转移2mole-,有0.25mol CH3COO-被氧化 | |
| C. | 当外电路中有2mole-转移时,进入A极区的H+的个数为2NA | |
| D. | A极的电极反应式为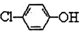 +H++e-═Cl-+ +H++e-═Cl-+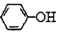 |
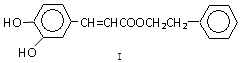

 或
或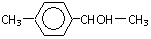 (写1种);由Ⅳ生成Ⅱ的反应条件为NaOH醇溶液、加热.
(写1种);由Ⅳ生成Ⅱ的反应条件为NaOH醇溶液、加热.