题目内容
下列离子方程式正确的是( )
| A、向盐酸中滴加氨水:H++OH-=H2O |
| B、Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
| C、铜溶于稀硝酸:3Cu+8H++2NO3-=3Cu2++2 NO↑+4H2O |
| D、CuSO4溶液与Ba(OH)2溶液混合:Cu2++SO42-+2OH-+Ba2+=BaSO4↓+Cu(OH)2↓ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.弱电解质写化学式;
B.二者发生氧化还原反应生成亚铁离子和碘;
C.二者反应生成硝酸铜、NO和水;
D.二者反应生成硫酸钡沉淀和氢氧化铜沉淀.
B.二者发生氧化还原反应生成亚铁离子和碘;
C.二者反应生成硝酸铜、NO和水;
D.二者反应生成硫酸钡沉淀和氢氧化铜沉淀.
解答:
解:A.弱电解质写化学式,离子方程式为H++NH3?H2O═NH4++H2O,故A错误;
B.二者发生氧化还原反应生成亚铁离子和碘,离子方程式为2Fe(OH)3+3H++2I-═2Fe2++3H2O+I2,故B错误;
C.二者反应生成硝酸铜、NO和水,离子方程式为3Cu+8H++2NO3-=3Cu2++2 NO↑+4H2O,故C正确;
D.二者反应生成硫酸钡沉淀和氢氧化铜沉淀,离子方程式为Cu2++SO42-+2OH-+Ba2+=BaSO4↓+Cu(OH)2↓,故D正确;
故选CD.
B.二者发生氧化还原反应生成亚铁离子和碘,离子方程式为2Fe(OH)3+3H++2I-═2Fe2++3H2O+I2,故B错误;
C.二者反应生成硝酸铜、NO和水,离子方程式为3Cu+8H++2NO3-=3Cu2++2 NO↑+4H2O,故C正确;
D.二者反应生成硫酸钡沉淀和氢氧化铜沉淀,离子方程式为Cu2++SO42-+2OH-+Ba2+=BaSO4↓+Cu(OH)2↓,故D正确;
故选CD.
点评:本题考查离子方程式正误判断,为高考高频点,明确物质的性质及离子方程式书写规则即可解答,注意B中氢氧化铁和HI不是单纯的酸碱中和反应,还发生氧化还原反应,为易错点,题目难度中等.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、非金属氧化物一定不是碱性氧化物 |
| B、HCl、H2S、NH3都是电解质 |
| C、漏斗、蒸馏烧瓶、分液漏斗、滴定管等仪器常用于物质分离 |
| D、Fe(OH)3、FeCl2、CuS都不能直接用化合反应制备 |
摩尔是( )
| A、计量微观粒子的物质的量的单位 |
| B、表示物质质量的单位 |
| C、国际单位制的一个基本物理量 |
| D、表示6.02×1023个粒子的集体 |
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
| A、Al2(SO4)3溶液呈酸性的原因是Al3+水解,离子方程式为:Al3++3OH-═Al(OH)3 |
| B、以KOH溶液为电解质溶液的氢氧燃料电池的负极反应式:O2+2H2O+4e-═4OH- |
| C、测0.1mol/L氨水的pH为11:NH3?H2O?NH4++OH- |
| D、钢铁发生吸氧腐蚀的正极反应式:Fe-2e-═Fe2+ |
下列说法中,正确的是( )
| A、化学家可以制造出自然界中不存在的物质 |
| B、化学研究的主要目的就是认识分子 |
| C、化学科学与其他科学分支的联系不密切 |
| D、化学研究会造成严重的环境污染,最终人类将毁灭在化学物质中 |
X、Y两元素可形成X2Y3型化合物,则X、Y原子基态时价电子的电子排布不可能是( )
| A、X:3d64s2 Y:2s22p4 |
| B、X:2s22p3Y:2s22p4 |
| C、X:3s23p1Y:3s23p4 |
| D、X:3s2Y:3s23p5 |
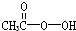 )是广为使用的消毒剂.它可由H2O2和冰醋酸反应制取,所以在过氧乙酸中常含有残留的H2O2.测定产品中过氧乙酸浓度c0.涉及下列反应:
)是广为使用的消毒剂.它可由H2O2和冰醋酸反应制取,所以在过氧乙酸中常含有残留的H2O2.测定产品中过氧乙酸浓度c0.涉及下列反应: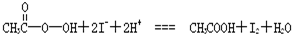
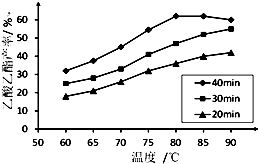 工业上常利用醋酸和乙醇合成有机溶剂乙酸乙酯:
工业上常利用醋酸和乙醇合成有机溶剂乙酸乙酯: