题目内容
下列关于离子反应及离子共存的说法中正确的是( )
| A、能使甲基橙显红色的溶液中,Ba2+、Fe2+、Cl-、NO3-可以大量共存 |
| B、钢铁发生吸氧腐蚀的正极反应:O2+4e-+4H+=2H2O |
| C、常温下,由水电离的c(H+)=10-12mol/L的溶液:K+、Na+、SiO32-、HCO3-可以大量共存 |
| D、NaHCO3溶液中滴入少量Ca(OH)2溶液:Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O |
考点:离子共存问题
专题:
分析:A.使甲基橙显红色的溶液呈酸性;
B.正极发生还原反应生成OH-;
C.由水电离的c(H+)=10-12mol/L的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性;
D.NaHCO3溶液中滴入少量Ca(OH)2溶液生成碳酸钙和碳酸钠.
B.正极发生还原反应生成OH-;
C.由水电离的c(H+)=10-12mol/L的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性;
D.NaHCO3溶液中滴入少量Ca(OH)2溶液生成碳酸钙和碳酸钠.
解答:
解:A.使甲基橙显红色的溶液呈酸性,酸性条件下Fe2+、NO3-发生氧化还原反应而不能大量共存,故A错误;
B.钢铁在中性、碱性条件下发生吸氧腐蚀,正极发生还原反应生成OH-,电极方程式为O2+4e-+2H2O=4OH-,故B错误;
C.由水电离的c(H+)=10-12mol/L的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性,无论呈酸性还是碱性,HCO3-都不能大量共存,故C错误;
D.NaHCO3溶液中滴入少量Ca(OH)2溶液生成碳酸钙和碳酸钠,反应的离子方程式为Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O,故D正确.
故选D.
B.钢铁在中性、碱性条件下发生吸氧腐蚀,正极发生还原反应生成OH-,电极方程式为O2+4e-+2H2O=4OH-,故B错误;
C.由水电离的c(H+)=10-12mol/L的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性,无论呈酸性还是碱性,HCO3-都不能大量共存,故C错误;
D.NaHCO3溶液中滴入少量Ca(OH)2溶液生成碳酸钙和碳酸钠,反应的离子方程式为Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O,故D正确.
故选D.
点评:本题综合考查离子共存、离子方程式的书写,为高频考点,侧重于学生的分析能力的考查,注意把握离子的性质以及反应类型的判断,难度不大.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
在容积相同的甲、乙两个密闭容器中,分别充入1mol N2、3mol H2,使它们在温度相同的条件下反应,并达到平衡.若甲容器保持体积不变,乙容器保持压强不变,平衡时甲容器中N2的转化率为10%,则乙容器中N2的转化率为( )
| A、10% | B、大于10% |
| C、小于10% | D、5% |
与乙炔具有相同的碳、氢百分含量,但一定既不是它的同系物又不是它的同分异构体的是( )
| A、丙炔 |
| B、乙烯 |
| C、C4H4 |
| D、苯 |
下列分子式表示的物质中,具有同分异构体的是( )
| A、C2H5Cl |
| B、C3H8 |
| C、CH2Cl2 |
| D、C2H6O |
下列关于有机化合物组成与结构判断正确的是( )
| A、有机物一定都含碳、氢元素 |
| B、分子中含有羟基的化合物属于醇类 |
| C、分子式相同,各元素质量分数也相同的物质是同种物质 |
| D、有机物分子中,氢原子数不一定都是偶数 |
为海底作业提供氧气的物质是( )
| A、KClO3 |
| B、KMnO4 |
| C、Na2O2 |
| D、H2O |
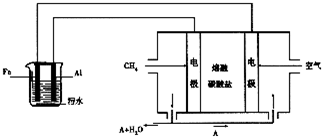 电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用电浮选凝聚法处理污水,设计装置如图所示:
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用电浮选凝聚法处理污水,设计装置如图所示: