题目内容
向体积为VL的NaALO2溶液中,开始通入amolHCl气体,则有bmol沉淀析出,继续通入cmolHCl气体后,产生的沉淀又恰好溶解,则原NaAlO2溶液的物质的量浓度是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
考点:离子方程式的有关计算
专题:计算题
分析:NaALO2溶液中通入HCl气体,生成氢氧化铝,继续通入HCl气体后,产生的沉淀又恰好溶解,发生反应为:AlO2-+4H+=Al3++H2O,根据相关的量来计算.
解答:
解:设有NaAlO2的物质的量为xmol,NaALO2溶液中通入HCl气体,生成氢氧化铝,继续通入HCl气体后,产生的沉淀又恰好溶解,发生反应为:
AlO2-+4H+=Al3++H2O,
1mol 4mol
xmol (a+c)mol
则
=
所以x=
;所以原NaAlO2溶液的物质的量浓度是
mol/L,
故选C.
AlO2-+4H+=Al3++H2O,
1mol 4mol
xmol (a+c)mol
则
| 1 |
| x |
| 4 |
| a+c |
所以x=
| a+c |
| 4 |
| a+c |
| 4V |
故选C.
点评:本题考查偏铝酸盐与酸反应的相关计算,题目难度中等,本题的解答关键是根据偏铝酸盐溶液中滴入盐酸生成沉淀再加盐酸与偏铝酸根先反应后与氢氧化铝反应,结合反应的有关方程式计算.

练习册系列答案
相关题目
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、0.1mol Cl2与足量NaOH溶液反应,转移电子的数目为0.2NA |
| B、0.1mol苯乙烯中含有碳碳双键的数目为0.4NA |
| C、标准状况下,11.2L乙醇中含有羟基的数目为0.5NA |
| D、4.6g由NO2和N2O4组成的混合物中含有氧原子的数目为0.2NA |
下列属于放热反应的是( )
| A、浓硫酸的稀释 |
| B、铝热反应 |
| C、氢气还原氧化铜 |
| D、Ba(OH)2?2H2O和NH4Cl(固体)混合 |
下列有关化学用语表示正确的是( )
A、氮气的电子式: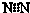 | ||
B、羟基的电子式: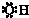 | ||
C、氯离子的结构示意图: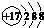 | ||
D、质子数为92、中子数为146的铀(U)原子的核素符号:
|
 请回答下列问题
请回答下列问题
 矿物透闪石是制作玉器的一种原料,其化学式可用CaxMgySi8O22(OH)m表示.
矿物透闪石是制作玉器的一种原料,其化学式可用CaxMgySi8O22(OH)m表示.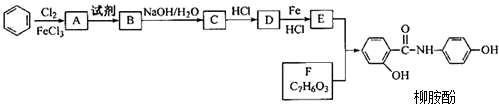
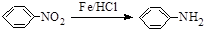 .请回答下列问题:
.请回答下列问题: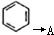 的化学方程式
的化学方程式