题目内容
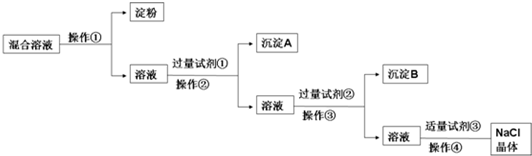
NaCl溶液中混有Na2SO4、CaCl2溶液和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体.相应的实验过程如图:
(1)写出上述实验过程中所用试剂(写化学式):
试剂① ;试剂③ .
(2)判断试剂①已过量的方法是: .
(3)用化学方程式表示加入试剂②的作用:
(4)操作①是利用半透膜进行分离提纯.操作①的实验结果:淀粉 (填“能”或“不能”)透过半透膜;SO42- (填“能”或“不能”)透过半透膜;请用实验证明上述结果,完成下表(可不填满,也可增加):限选试剂:1mol/L AgNO3溶液、1mol/L BaCl2溶液、1mol/L Ba(NO3)2溶液、碘水、稀盐酸、稀硝酸

(1)写出上述实验过程中所用试剂(写化学式):
试剂①
(2)判断试剂①已过量的方法是:
(3)用化学方程式表示加入试剂②的作用:
(4)操作①是利用半透膜进行分离提纯.操作①的实验结果:淀粉
| 编号 | 实验操作 | 预期现象和结论 |
| ① | ||
| ② | ||
考点:物质分离和提纯的方法和基本操作综合应用
专题:实验题
分析:胶体不能透过半透膜,操作①为渗析,除去Na2SO4、CaCl2,可分别加入BaCl2、Na2CO3,除去粗盐中含有的Ca2+、SO42-可溶性杂质的方法:加入过量BaCl2,去除硫酸根离子;再加入过量Na2CO3(去除钙离子),则试剂①为BaCl2,操作②为过滤,沉淀A为硫酸钡,试剂②为Na2CO3,操作③为过滤,沉淀B为碳酸钙和碳酸钡,试剂③为盐酸,加入盐酸可除去过量的Na2CO3,最后蒸发结晶可得到NaCl晶体,以此解答该题.
解答:
解:胶体不能透过半透膜,操作①为渗析,除去Na2SO4、CaCl2,可分别加入BaCl2、Na2CO3,除去粗盐中含有的Ca2+、SO42-可溶性杂质的方法:加入过量BaCl2,去除硫酸根离子;再加入过量Na2CO3(去除钙离子),则试剂①为BaCl2,操作②为过滤,沉淀A为硫酸钡,试剂②为Na2CO3,操作③为过滤,沉淀B为碳酸钙和碳酸钡,试剂③为盐酸,加入盐酸可除去过量的Na2CO3,最后蒸发结晶可得到NaCl晶体,
(1)由以上分析可知试剂①为BaCl2,试剂③为HCl,故答案为:BaCl2;HCl;
(2)判断试剂①已过量的方法是静置,向上层清液中滴加少量氯化钡溶液,没有白色沉淀产生,说明氯化钡溶液已过量,
故答案为:静置,向上层清液中滴加少量氯化钡溶液,没有白色沉淀产生,说明氯化钡溶液已过量;
(3)试剂②为Na2CO3,加入试剂②的作用是除去溶液中钙离子和过量的钡离子,反应的化学方程式为BaCl2+Na2CO3=2NaCl+BaCO3↓、CaCl2+Na2CO3=2NaCl+CaCO3↓,
故答案为:BaCl2+Na2CO3=2NaCl+BaCO3↓、CaCl2+Na2CO3=2NaCl+CaCO3↓;
(4)胶体粒子和浊液粒子半径比较大,不能透过半透膜,而溶质粒子可通过半透膜,
检验淀粉,可取半透膜外液体,加入少量碘水,液体没有变成蓝色,证明淀粉不能透过半透膜,检验SO42-,可另取半透膜外液体,加入足量稀盐酸和少量1mol/L BaCl2溶液,产生不溶于盐酸的白色沉淀,证明SO42-能够透过半透膜.
故答案为:不能; 能;
(1)由以上分析可知试剂①为BaCl2,试剂③为HCl,故答案为:BaCl2;HCl;
(2)判断试剂①已过量的方法是静置,向上层清液中滴加少量氯化钡溶液,没有白色沉淀产生,说明氯化钡溶液已过量,
故答案为:静置,向上层清液中滴加少量氯化钡溶液,没有白色沉淀产生,说明氯化钡溶液已过量;
(3)试剂②为Na2CO3,加入试剂②的作用是除去溶液中钙离子和过量的钡离子,反应的化学方程式为BaCl2+Na2CO3=2NaCl+BaCO3↓、CaCl2+Na2CO3=2NaCl+CaCO3↓,
故答案为:BaCl2+Na2CO3=2NaCl+BaCO3↓、CaCl2+Na2CO3=2NaCl+CaCO3↓;
(4)胶体粒子和浊液粒子半径比较大,不能透过半透膜,而溶质粒子可通过半透膜,
检验淀粉,可取半透膜外液体,加入少量碘水,液体没有变成蓝色,证明淀粉不能透过半透膜,检验SO42-,可另取半透膜外液体,加入足量稀盐酸和少量1mol/L BaCl2溶液,产生不溶于盐酸的白色沉淀,证明SO42-能够透过半透膜.
故答案为:不能; 能;
| 编号 | 实验操作 | 预期现象和结论 |
| ① | 取半透膜外液体,加入少量碘水 | 液体没有变成蓝色,证明淀粉不能透过半透膜 |
| ② | 另取半透膜外液体,加入足量稀盐酸和少量1mol/L BaCl2溶液 | 产生不溶于盐酸的白色沉淀,证明SO42-能够透过半透膜 |
点评:本题考查物质的分离提纯操作,题目难度中等,本题注意Ca2+、SO42-的性质,把握除杂原则,提纯时不能引入新的杂质,注意把握实验的先后顺序.

练习册系列答案
相关题目
NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、1molCl2发生反应时,转移的电子数一定为2NA |
| B、1.7g H2O2中含有的电子数为0.9 NA |
| C、1mol Na2O2 固体中含离子总数为4 NA |
| D、标准状况下,2.24L苯所含分子数为0.1NA |
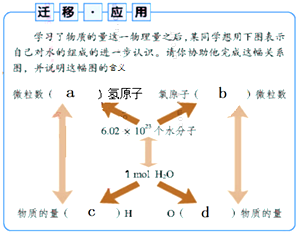 如图所示为鲁科版化学教科书(我们正在使用的教科书)必修1中“迁移应用”栏目的一个学习活动.下列关于a、b、c、d处所填内容及这幅图含义的描述中,不正确的是( )
如图所示为鲁科版化学教科书(我们正在使用的教科书)必修1中“迁移应用”栏目的一个学习活动.下列关于a、b、c、d处所填内容及这幅图含义的描述中,不正确的是( )| A、a=1.204×1024、b=6.02×1023、c=2、d=1 |
| B、6.02×1023个H2O水分子中含有1.204×1024个氢原子和6.02×1023个氧原子 |
| C、1mol H2O中含有2mol H和1mol O |
| D、对于同一微粒,其物质的量与微粒数间可通过阿伏加德罗常数实现相互换算 |
下列关于胶体的叙述正确的是( )
| A、向1 mol?L-1氯化铁溶液中加入少量的NaOH溶液制取氢氧化铁胶体 |
| B、可以用丁达尔现象区别硫酸铜溶液和氢氧化铁胶体 |
| C、氢氧化铁胶体通电后氢氧化铁胶粒向正极移动 |
| D、由0.1mol氯化铁制取的氢氧化铁胶体中,氢氧化铁胶粒数目为0.1NA(设NA表示阿伏加德罗常数的值) |
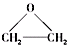 ),该反应的原子利用率为100%,反应的化学方程式为
),该反应的原子利用率为100%,反应的化学方程式为