题目内容
4.图是一些常见单质、化合物之间的转化关系图,有些反应中的部分物质被略去.常温常压下,A为无色有毒气体,B为红棕色粉末,C、E为金属单质,G、J的焰色均为黄色.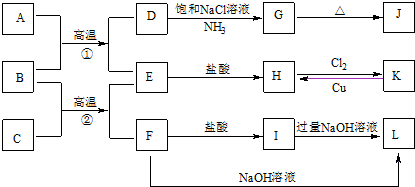
请回答下列问题:
(1)G的化学式为NaHCO3,D的电子式为
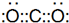 .
.(2)F→L反应的化学方程式为Al2O3+2NaOH=2NaAlO2+H2O.
(3)K→H是制作印刷电路板的重要反应,该反应的离子方程式为2Fe3++Cu=2Fe2++Cu2+.
分析 B为红棕色粉末,则B为Fe2O3,A为无色有毒气体,结合转化关系,可推知A具有还原性,故A为CO,则D为CO2,E为Fe,G为NaHCO3,J为Na2CO3,H是FeCl2,K为FeCl3,金属C与氧化铁反应生成Fe与F,F为金属氧化物,既与盐酸反应又能与氢氧化钠反应,则F为Al2O3,C是Al,I为AlCl3,L为NaAlO2,据此解答.
解答 解:B为红棕色粉末,则B为Fe2O3,A为无色有毒气体,结合转化关系,可推知A具有还原性,故A为CO,则D为CO2,E为Fe,G为NaHCO3,J为Na2CO3,H是FeCl2,K为FeCl3,金属C与氧化铁反应生成Fe与F,F为金属氧化物,既与盐酸反应又能与氢氧化钠反应,则F为Al2O3,C是Al,I为AlCl3,L为NaAlO2.
(1)G的化学式为NaHCO3,D为CO2,电子式为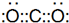 ,故答案为:NaHCO3;
,故答案为:NaHCO3;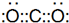 ;
;
(2)F→L反应的化学方程式为:Al2O3+2NaOH=2NaAlO2+H2O,故答案为:Al2O3+2NaOH=2NaAlO2+H2O;
(3)K→H的离子方程式为:2Fe3++Cu=2Fe2++Cu2+,故答案为:2Fe3++Cu=2Fe2++Cu2+.
点评 本题考查无机物的推断,B的颜色、A的性质及转化中F的性质为推断突破口,注意对基础知识的理解掌握.

练习册系列答案
相关题目
14.下列说法正确的是( )
| A. | BaO2(过氧化钡)固体中的阴离子和阳离子之比为2:1 | |
| B. | 在SiO2晶体中,1个Si原子和2个O原子形成2个共价键 | |
| C. | HCl的相对分子质量大于HF,所以HCl的沸点高于HF | |
| D. | 由ⅠA族和ⅥA族元素可形成原子个数比为1:1、电子总数为38的化合物 |
15.下列物质中既有离子键又有共价键的是( )
| A. | CaO | B. | CO2 | C. | K2O | D. | Ca(OH )2 |
12.下表列出了①~⑨九种元素在周期表中的位置:
请按要求回答下列问题.
(1)化学性质最不活泼的元素的原子结构示意图为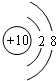
(2)⑥④⑦的氢化物的稳定性最强的是:H2O(写氢化物的化学式);
(3)元素③④⑤形成的离子半径由大到小的顺序是N3->O2->Na+(用离子符号表示)
(4)用电子式表示元素⑤与⑦的化合物的形成过程: .
.
| ⅠA | Ⅷ | ||||||
| ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| ② | ③ | ④ | ⑧ | ||||
| ⑤ | ⑥ | ⑦ | ⑨ | ||||
(1)化学性质最不活泼的元素的原子结构示意图为
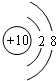
(2)⑥④⑦的氢化物的稳定性最强的是:H2O(写氢化物的化学式);
(3)元素③④⑤形成的离子半径由大到小的顺序是N3->O2->Na+(用离子符号表示)
(4)用电子式表示元素⑤与⑦的化合物的形成过程:
 .
.
19.NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 在某密闭容器中加入0.5molN2和1.5molH2,充分反应后容器中物质含有的N-H键数为3NA | |
| B. | 标准状况下,2.24LSO3含有的原子数为0.4 NA | |
| C. | 71g氯气与足量铁反应过程中转移的电子数为2NA | |
| D. | 电解饱和食盐水时,当阴极产生22.4LH2时,电路中转移的电子数为2NA |
9.25℃,pH=2的 HC1溶液中,由水电离出的c(H+)是( )
| A. | 1×10-7 mol/L | B. | 1×10-12mol/L | C. | 1×10-2 mol/L | D. | 1×10-7 mol/L |
13.用惰性电极电解一定浓度的CuSO4溶液,通电一段时间后,向所得的溶液中加入0.1mol 的CuO和0.1molH2O后恰好恢复到电解前的浓度,则电解过程中阳极产生的气体在标准状况下的体积为( )
| A. | 2.24L | B. | 3.36L | C. | 1.12L | D. | 4.48L |
14.如图所示有机物的一氯取代物有(不含立体异构)( )
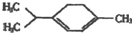

| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |
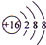
 2NH3,向X的水溶液中滴入酚酞溶液,会观察到溶液变红色
2NH3,向X的水溶液中滴入酚酞溶液,会观察到溶液变红色