题目内容
在给定条件下,下列加点的物质在化学反应中完全消耗的是( )
A、用50 mL 12 mol/L的
| ||||||
B、常温下,将1 g
| ||||||
C、向100 mL 3 mol/L的稀硝酸中加入5.6 g
| ||||||
D、常温常压下,0.1 mol
|
考点:化学方程式的有关计算,氯气的化学性质,硝酸的化学性质,浓硫酸的性质
专题:卤族元素,氧族元素,氮族元素
分析:A.加热条件下,浓盐酸和MnO2反应生成Cl2,但稀盐酸和MnO2不反应;
B.常温下,Al和浓硫酸发生钝化现象;
C.5.6gFe的物质的量=
=0.1mol,n(HNO3)=3mol/L×0.1L=0.3mol,二者反应方程式为3Fe+8HNO3=3Fe(NO3)3+2NO↑+4H2O、Fe+4HNO4=Fe(NO3)3+NO↑+2H2O,
<n(Fe):n(HNO4)=0.1mol:0.3mol=
<
,所以铁完全反应,硝酸有剩余;
D.常温常压下,1L水中能溶解2L氯气.
B.常温下,Al和浓硫酸发生钝化现象;
C.5.6gFe的物质的量=
| 5.6g |
| 56g/mol |
| 1 |
| 4 |
| 1 |
| 3 |
| 3 |
| 8 |
D.常温常压下,1L水中能溶解2L氯气.
解答:
解:A.加热条件下,浓盐酸和MnO2反应生成Cl2,但稀盐酸和MnO2不反应,当浓盐酸浓度达到一定程度后变为稀盐酸后不再和二氧化锰反应,所以氯化氢不能完全转化,故A错误;
B.常温下,Al和浓硫酸发生氧化还原反应生成一层致密的氧化物薄膜而阻止进一步被氧化,所以Al不能完全消耗,故B错误;
C.5.6gFe的物质的量=
=0.1mol,n(HNO3)=3mol/L×0.1L=0.3mol,二者反应方程式为3Fe+8HNO3=3Fe(NO3)3+2NO↑+4H2O、Fe+4HNO3=Fe(NO3)3+NO↑+2H2O,
<n(Fe):n(HNO4)=0.1mol:0.3mol=
<
,所以铁完全反应,硝酸有剩余,铁被氧化生成亚铁离子和铁离子,故C正确;
D.常温常压下,0.1mol氯气的体积是2.24L,1L水中能溶解2L氯气,所以氯气不能完全溶解,故D错误;
故选C.
B.常温下,Al和浓硫酸发生氧化还原反应生成一层致密的氧化物薄膜而阻止进一步被氧化,所以Al不能完全消耗,故B错误;
C.5.6gFe的物质的量=
| 5.6g |
| 56g/mol |
| 1 |
| 4 |
| 1 |
| 3 |
| 3 |
| 8 |
D.常温常压下,0.1mol氯气的体积是2.24L,1L水中能溶解2L氯气,所以氯气不能完全溶解,故D错误;
故选C.
点评:本题考查物质之间的反应,明确物质的性质是解本题关键,注意酸的浓度不同其性质不同,注意C选项中要结合方程式分析,题目难度中等.

练习册系列答案
相关题目
铜易生锈,铜合金更易生锈,铜器上往往覆盖着一层铜绿,铜绿的主要成分是( )
| A、CuO |
| B、Cu(OH)2 |
| C、Cu2O |
| D、Cu2(OH)2CO3 |


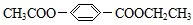 如图是A、B分别经①、②两步反应得到各种产物的相互关系示意图,请回答下列问题:
如图是A、B分别经①、②两步反应得到各种产物的相互关系示意图,请回答下列问题: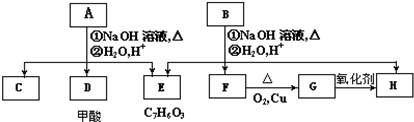
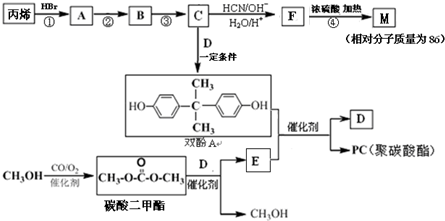
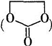 能与CH3OH发生酯交换反应生成碳酸二甲酯和另一种醇,写出该反应的化学方程式
能与CH3OH发生酯交换反应生成碳酸二甲酯和另一种醇,写出该反应的化学方程式